Biologiske legemidler og biosimilars
Tekst: Jo Klaveness, Farmasøytisk institutt, Universitetet i Oslo
Last ned atikkelen i pfd-format.
Det har siden tusenårsskiftet kommet mange nye såkalte «biologiske legemidler». Disse legemidlene, som inneholder svært kompliserte virkestoffer, har vist seg å ha stor klinisk nytteverdi. Legemidlene er generelt kostbare, og mange av dem er blant de mest omsatte legemidlene, både i Norge og resten av verden. Den senere tiden har det også kommet flere såkalte biotilsvarende legemidler eller biosimilars.
Legemidler og virkestoffer
Alle legemidler i klinisk bruk består av ett eller flere virkestoff(er) samt ett eller flere hjelpestoff(er). Et virkestoff betegnes ofte som «drug substance» eller «active pharmaceutical ingredient», forkortet «API» og hele legemiddelet som «drug product». Det var i 2011 nærmere 1500 ulike virkestoffer i klinisk bruk i Norge, mens antallet legemidler med markedsføringstillatelse var over 13 000.
Det er den kjemiske formel eller kjemiske struktur av virkestoffet som bestemmer legemiddelets biologiske profil; herunder både terapeutisk effekt og bivirkningsprofil. Virkestoffer med ulik biologisk profil har derfor svært ulik kjemisk struktur. Denne sammenhengen mellom kjemisk struktur og biologisk profil er et sentralt tema innenfor fagområdet legemiddelkjemi og i farmasien generelt. Figur 1 viser kjemisk formel for to virkestoffer; paracetamol og losartan.
Slike virkestoffer omtales ofte som «kjemiske virkestoffer» og fremstilles ved en syntetisk prosess, ved en semisyntetisk prosess (naturstoffer som syntetisk modifiseres til ønsket virkestoff) eller isoleres fra en naturlig kilde som en mikroorganisme eller en plante. Eksempler på slike naturprodukter er flere antibiotika, og typiske eksempler på semisyntetiske virkestoffer er steroider og de fleste penicilliner. De fleste legemiddelsubstanser, som for eksempel paracetamol og losartan, fremstilles imidlertid syntetisk.
Alle disse såkalte kjemiske virkestoffene er relativt enkle lavmolekylære stoffer. Paracetamol inneholder 8 karbonatomer og har en molekylvekt på 151 Dalton, mens losartan er et noe mer komplisert molekyl med en molekylvekt på 423 Dalton. De fleste virkestoffer har molekylvekt mindre enn 500 Dalton, men det finnes flere substanser som har betydelig høyere molekylvekt.
Syntetiske virkestoffer kan vanligvis fremstilles ved alternative synteseruter. Dette betyr at utgangsmaterialene (byggesteinene) kan være forskjellige, de kjemiske prosesser kan være forskjellige og antall prosesstrinn kan være forskjellige. Sluttproduktet er imidlertid identisk, dog kan virkestoffene ha noe ulik forurensningsprofil, men dette har ingen klinisk eller regulatorisk betydning da forurensningene er til stede i svært små menger.
De ulike syntetiske prosessene gir altså identiske virkestoffer.
Hva menes med et generisk legemiddel?
Generisk likeverdige legemidler er «synonyme preparater» som vil si legemidler med samme virkestoff, samme legemiddelform og samme styrke. Vi bruker betegnelsen generisk legemiddel om legemidler som ikke er patentbeskyttet og som dermed kan produseres og markedsføres av ulike legemiddelselskaper.
Ellers like legemidler inneholdende for eksempel losartan fremstilt ved ulike kjemiske syntetiske synteseveier, vil dermed være typiske generiske legemidler da virkestoffet er «det samme», altså identisk, og ikke lenger er patentbeskyttet.
Mange generiske legemidler står på den såkalte byttelisten. Denne listen over legemidler, som er byttbare i apotek, utarbeides av Statens legemiddelverk og baserer seg på at legemidlene er generiske og er medisinsklikeverdige. I vurderingen av medisinsk likeverdighet vurderes blant annet biotilgjengelighetsstudier samt doseringsanvisning og risiko for feilbruk.
De aller fleste legemidlene i Norge i dag med markedsføringstillatelse er generiske legemidler.
Hva menes med et biologisk legemiddel?
«Biologiske legemidler» er legemidler som inneholder virkestoffer som er fremstilt av levende organismer eller renset fra levende organismer. Antibiotika og andre lavmolekylære substanser som isoleres fra levende organismer går imidlertid ikke under betegnelsen biologiske legemidler. Typiske biologiske legemiddelsubstanser er proteiner og protein-derivater samt enkelte andre store kroppsegne molekyler. Selv om vi betegner disse legemiddelsubstansene som biologiske legemidler er jo disse selvfølgelig også kjemiske substanser. Alle legemiddelsubstanser er kjemiske substanser; forskjellen er at de biologiske legemiddelsubstansene er store molekyler som er fremstilt i levende organismer. Den enkleste biologiske legemiddelsubstansen er humant insulin som er et stort peptid eller et lite protein med molekylvekt 5808 Dalton. Molekylvekten for et typisk biologisk legemiddel er vanligvis mye høyere. Flere biologiske legemiddelsubstanser har molekylvekt omkring 150 000 Dalton, hvilket er tusen ganger mer enn molekylvekten for paracetamol. Molekylvekten er et godt mål for en legemiddelsubstans’ kompleksitet.
Hva er et protein?
Betegnelsen protein bruker vi i hverdagen sammen med fett og karbohydrat når vi snakker om næringsstoffene i matvarer. Høyt innhold av protein regnes i dagligtale, i motsetning til fett og karbohydrat, som generelt positivt i næringsmidler.
I kroppen vår har vi en rekke spesielle proteiner med helt spesielle biologiske funksjoner.
Et protein er kjemisk bygget opp av byggesteiner som vi kaller aminosyrer. En aminosyre er en kjemisk substans inneholdende en såkalt amino-gruppe og en karboksylsyre-gruppe. Figur 2 viser kjemisk formel for to aminosyrer og hvorledes disse kan koples sammen, som videre kan koples til nye aminosyrer slik at det dannes en kjede.
Når to eller flere aminosyrer koples sammen til kjeder kaller vi dette et peptid og en lang peptidkjede betegner vi som et protein. Det finnes 20 ulike aminosyrer som danner basis for peptider og proteiner som naturlig er til stede i kroppen vår. Figur 3 viser en skisse av insulin som beståender av 51 aminosyrer koplet sammen i to kjeder som igjen er sammenkoplede. Hver sirkel beskriver en aminosyre.
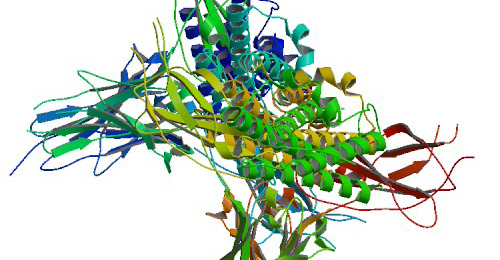
Aminosyrene har ulike sidekjeder som gir peptidene og proteinene forskjellige kjemiske og biologiske egenskaper. Noen sidekjeder er hydrofile (liker vann), andre er hydrofobe (liker ikke vann) mens andre igjen er ladet (positiv eller negativ ladning). De ulike sidekjedene kan ha affinitet til hverandre og danne ulike former for bindinger i proteinet, noe som fører til at et større protein i løsning i kroppen vår ikke ser ut som «et langt perlekjede», men mer som et «rotete garnnøste» som vist på figur 4.
Proteiner er kompliserte kjemiske strukturer som kan folde seg på flere måter avhengig av en rekke parametere. Vi pleier vanligvis å beskrive proteinene ved hjelp av såkalt primærstruktur, sekundærstruktur, tertiærstruktur og kvarternær struktur. Primærstrukturen forteller oss hvilke aminosyrer som er til stede og rekkefølgen for hvorledes disse er koplet sammen, mens de øvrige strukturer beskriver de romlige aspekter av «det rotete garnnøstet» på ulike nivåer. Det er den totale romlige strukturen som bestemmer proteinets biologiske funksjon.
Hva brukes biologiske legemidler til?
Biologiske legemidler brukes i dag for behandling av en rekke sykdomstilstander; spesielt innen onkologien og immunologiske sykdommer. De enkleste biologiske legemiddelsubstansene er insulin og insulin-derivater som brukes for behandling av diabetes. De mest komplekse biologiske legemidlene er de såkalte monoklonale antistoffene («Mabs») som blant annet brukes i behandling av ulike kreftformer. Mange av de mest omsatte legemidlene i Norge og i resten av verden er biologiske legemidler. Tabell 1 viser en kronologisk oversikt over de 14 mest omsatte biologiske legemiddelsubtansene på det norske marked, listet etter avtakende omsetning. Etanercept (Enbrel) var det mest omsatte virkestoffet med en omsetning på 437 millioner NOK i Norge i 2011. Disse 14 biologiske legemidlene var blant de 50 mest omsatte legemidlene og omsatte alle for over 70 millioner NOK i Norge i 2011.
Alle legemidlene administreres parenteralt da virkestoffene er kompliserte molekyler som har liten eller ingen biotilgjengelighet ved oral administrasjon. Vanligvis leveres biologiske legemiddelsubstanser som frysetørket pulver eller i form av en løsning som eventuelt skal fortynnes før bruk. Alle biologiske legemidler er i form av sterile produkter. Biologiske legemidler har spesielle utfordringer relatert til formulering av de proteinbaserte virkestoffene. Proteiner kan være kjemisk og fysikalsk relativt ustabile forbindelser, noe som gjør at de farmasøytiske utfordringene, med å utvikle egnede farmasøytiske formuleringer, ofte er betydelig større enn for tradisjonelle kjemiske legemiddelsubstanser. Utfordringene med formulering av biologiske legemidler er blant annet relatert til aggregering og utfelling av proteiner i løsningene, fremstilling av egnet frysetørket pulver som lett kan løses opp til ønsket produkt før bruk og generelt stabilitet av produktet både i form av pulver og i løsning.
Alle legemidler kan gi bivirkninger. Den største generelle bekymringen ved klinisk bruk av alle biologiske legemidler er faren for immunologiske reaksjoner. En slik reaksjon kan være alvorlig og det er vanskelig eller umulig å forutsi at en slik uønsket reaksjon kan oppstå. Substanser med et immunologisk potensial er ofte store molekyler eller reaktive substanser som kan reagere med kroppsegne substanser som proteiner.
Hvordan fremstilles biologiske legemidler?
Biologiske legemidler kan i utgangspunktet isoleres fra biologisk materiale. Det er imidlertid normalt svært kostbart og har en rekke regulatoriske og etiske aspekter. Innen moderne bioteknologi har det blitt utviklet en metode som kalles for rekombinant DNA-teknologi. Svært kort fortalt, betyr dette at den del av det humane DNA som koder for et spesielt humant protein «klippes ut» av det humane DNA og for eksempel «limes inn» i bakterie-DNA. Ved dyrking av bakteriene inneholdende det modifiserte bakterie-DNA vil disse bakteriene være i stand til å produsere det humane proteinet i store mengder. Selve prosessen foregår i såkalte bioreaktorer hvor cellene har optimale forhold for å produsere det humane proteinet. Det humane proteinet isoleres, renses og bearbeides videre i en omfattende prosess for så at proteinet formuleres til den endelige sterile legemiddelformuleringen. Fordelene med å bruke rekombinant DNA-teknologi i fremstilling av humane proteiner er flere:
- Man får tilgang til store menger riktig protein i en industriell prosess.
- Det er ikke behov for større mengder biologisk materiale.
- Der er ikke fare forkontaminering med sykdomsfremkallende materiale.
- Det er en kostnadseffektiv prosess.
I motsetning til produkter som fremkommer i syntetiske prosesser er, imidlertid, produktet som dannes ved en biologisk prosess svært avhengig av prosessen. Selv om to protein har den samme aminosyresekvens, kan de to produkter fra to ulike prosesser resultere i proteiner med noe ulik struktur.
Den kjemiske romlige struktur av et protein kan bestemmes ved bruk av en avansert metode som kalles røntgenkrystallografi. Ved bruk av en slik metode kan strukturen av proteinet i krystallinsk tilstand bestemmes helt nøyaktig. Alle legemiddelsubstanser er, imidlertid, i løsning in vivo, og det er interaksjonen med det biologiske target når legemiddelsubstansen er i løsning som er av betydning for de farmakologiske og toksikologiske effekter. Det finnes i dag ingen metode for direkte å bestemme biologiske legemidlers struktur i løsning. Dette ville i så fall vært et svært nyttig verktøy for å oppnå en enda bedre forståelse av legemidlers virkemåte.
Hva er biosimilars?
Biosimilars eller tilsvarende biologiske legemidler (biotilsvarende legemidler), som det heter med norsk terminologi, er biologiske legemidler som likner det originale biologiske legemiddelet. Videre i denne artikkelen bruker vi de ulike navnene om hverandre. Slike tilsvarende biologiske legemidler har, når det gjelder proteiner, samme aminosyresekvens som original-legemiddelet, men det kan likevel være ulikheter relatert til den totale kjemiske strukturen. Da tilsvarende biologiske legemidler ikke er identiske kopier av det originale biologiske legemiddelet, er slike biotilvarende legemidler ikke generiske legemidler. All litteratur på området skiller i dag klart mellom generiske legemidler og biosimilars. Biotilsvarende legemidler vil, som følge av at de produseres av en annen produsent enn originalprodusenten, være produsert med en prosess, som likner originalprodusentens prosess men ikke er helt lik. Disse ulikhetene kan for eksempel være relatert til cellekultur, reaktortype, batchstørrelse, prosessbetingelser, renseprosesser og formulering.
Alle fremstillingsprosesser av virkestoffer gir generelt forurensninger. Disse forurensningene kan være til stede i legemiddelet i små mengder, og øvre grenseverdier for disse er en del av spesifikasjonene i monografier i blant annet Ph. Eur. Forurensningene i biologiske legemidler kan være små mengder fremmede proteiner. Biologiske legemidler fremstilt med ulike prosesser har potensial til å gi ulik forurensningsprofil; altså ulik profil av fremmede proteiner.
Det er i dag, ifølge Legemiddelverket, 12 biotilsvarende legemidler som har markedsføringstillatelse i Norge. Dette er seks produkter inneholdende filgrastim (Tevagrastim, Zarzio, Nivestim, Biograstim, Filgrastim Hexal og Ratiograstim), fem produkter inneholdende erytropoietin (Retacrit, Silapo, Abseamed, Epoetin alfa Hexal og Binocrit) samt ett produkt inneholdende somatropin (Omnitrope). Disse legemidlene er alle, i likhet med originalproduktene, sikre og effektive legemidler. Filgrastim er en såkalt kolonistimulerende faktor og brukes ved nøytropeni i forbindelse med cytostatikabehandling eller hos pasienter med fremskreden hivinfeksjon. Erytropoietin (epoetin alfa) er en legemiddelsubstans som brukes ved anemi, og somatroptin er et veksthormon som brukes ved vekstforstyrrelser. Somatropin er blant de biologiske legemidlene med størst omsetning (se tabell 1). Det er en rekke biotilsvarende legemidler som venter på enmarkedsføringstillatelse og enda flere som er sent i utviklingprosessen og dermed forventes å komme på markedet de nærmeste årene. Svært mange legemiddelprodusenter er interessert i biotilsvarende legemidler. Dette inkluderer både de tradisjonelle Big Pharma-selskapene, generiske legemiddelprodusenter og mindre legemiddelselskaper. Det foregår mye utvikling av biotilsvarende legemidler i Asia; spesielt i India, Korea og Kina.
Enkelte av selskapene som utvikler og produserer biosimilars arbeider med mulig forbedrede produkter som nå omtales som «biobetters» og «biosuperiors». Disse terminologier eksisterte knapt på Google for et par år siden!
Regulatorisk dokumentasjon av biosimilars
Europeiske legemiddelmyndigheter (EMA) var tidlig ute med å vurdere hvilken regulatorisk dokumentasjon som kreves for å oppnå markedsføringstillatelse for biosimilars. EMA har utarbeidet generelle guidelines for biosimilars og noen spesifikke guidelines for utvalgte grupper av biosimilars. Disse er tilgjengelig på EMAs hjemmesider. Et biotilsvarende legemiddel dokumenteres generelt ved at det gjøres direkte sammenliknende studier av originalprodukt og det biotilsvarende legemiddel hva gjelder kjemisk-farmasøytisk karakterisering, prekliniske studier (herunder forsøk i dyr) og kliniske studier. Når det gjelder kliniske studier er det ikke nødvendig å gjøre slike studier for alle indikasjonene som originalproduktet er godkjent for. Her kan det foretas en ekstrapolering mellom indikasjonene. Den regulatoriske dokumentasjonen av et biotilsvarende legemiddel er av betydelig mindre omfang enn dokumentasjonen som ligger bak originalproduktet, men den er betydelig mer omfattende, og forskjellig, fra den dokumentasjon som danner grunnlag for markedsføringstillatelser for generiske legemidler.
Hva skiller biosimilars fra generiske legemidler?
Generisk legemidler er legemidler som inneholder samme virkestoff som originalproduktet, mens biotilsvarende legemidler inneholder virkestoffer som likner på originalproduktet, men ikke er helt likt. Generiske legemidler er fremstilt ved en kjemisk prosess, mens biotilsvarende legemidler er fremstilt ved en biologisk prosess hvor det er levende celler som produserer virkestoffet. Legemiddelsubstansen som fremstilles i biologiske prosesser er svært avhengig av produksjonsprosessen, mens det ikke er tilfelle når det gjelder kjemiske prosesser. Her vil ikke prosessen være avgjørende for sluttproduktets struktur og funksjon. Generiske legemidler er enkle, små molekyler, mens biosimilars er kompliserte proteiner og protein-derivater.
Hvorfor er ikke biologiske legemidler på byttelisten i Norge?
Et biotilsvarende legemiddel er altså et biologisk legemiddel som likner det originale legemiddelet, men som ikke er, eller er vist å være, helt likt det biologiske originalproduktet. Da biotilsvarende legemidler dermed ikke er generisk likeverdige legemidler er det ikke grunnlag for bytte av biologiske legemidler i henhold til apotekloven i Norge. Dette er også bekreftet av Oslo tingrett i dom av 31. mars 2011.
Dokumentasjonskravene, som EMA har utarbeidet, omfatter sammenliknende immunogenisitetsstudier for biosimilar og originalproduktet, men det er ikke krav til at det skal utføres ikke kliniske immunogenisitetsstudier hvor produkter fra ulike leverandører med ulike produksjonsprosesser byttes en eller flere ganger for en og samme pasient. Det kan ved bytte være fare for kryssimmunitetsreaksjonersom muligens kan medføre tap av effekt og medføre bivirkninger. EMAs dokumentasjonskrav omfatter ingen studier relatert til bytte av biologiske legemidler.
Flere kliniske studier som omhandler bytte av biologiske legemidler er initiert, men i dag finnes det svært få eller ingen vitenskapelige artikler som beskriver bytte av biologiske legemidler.
Forfatteren kjenner ikke til noen land som praktiserer bytte i apotek av biologiske legemidler som er produsert med ulik produksjonsprosess.
Til slutt
Biologiske legemidler inneholder svært kompliserte virkestoffer i form av proteiner eller protein-derivater. Disse har vist seg å ha stor klinisk nytteverdi. Legemidlene er generelt kostbare og mange av dem er blant de mest omsatte legemidlene. Biosimilars er biologiske legemidler som likner det originale legemiddelet, men som ikke er, eller er vist å være, helt likt det biologiske originalproduktet. Biosimilars er ikke generiske legemidler og er dermed ikke byttbare i apotek. Det er ingen land som i dag praktiserer bytte av biologiske legemidler i apotek. Det foreligger lite eller ingen klinisk dokumentasjon av mulige effekter av bytte av biologiske legemidler.
I likhet med generiske legemidler vil det være flere biosimilars basert på ulike produksjonsprosesser tilgjengelige. Dette betyr at et eventuelt bytte i apotek kan skje mellom flere ulike produkter slik at man kan få en situasjon hvor en enkelt pasient til stadighet bytter mellom flere ulike biologiske legemidler.
For at et biologiske legemiddel skal kunne byttes i apotek må det foreligge grundig klinisk dokumentasjon for dette spesifikke produktbytte i den relevante pasientgruppen. Slik klinisk dokumentasjon gjøres i kontrollerte kliniske studier og vil bli publisert i internasjonale fagtidsskrifter.
Eventuelt bytte av biologiske legemidler i apotek må derfor basere seg på studier administrert av kliniske utprøvere og ikke av innkjøpere i norske apotekkjeder og Legemiddelinnkjøpssamarbeidet (LIS).
(Publisert i NFT nr. 1/2013 side 22–25.)
