Betydning av CYP2C19-genetikk for SSRI-preparater
Doktoravhandling
Tittel
Impact of CYP2C19genetics on pharmacokinetic variability of escitalopram and sertraline – a study based on therapeutic drug monitoring data
Emne
Farmakologi, farmakogenetikk
Stipendiat
Ida Rudberg, Senter for Psykofarmakologi (tidligere Psykofarmakologisk avdeling), Diakonhjemmet Sykehus
idarudberg@gmail.com
Hovedveileder
Espen Molden, Senter for Psykofarmakologi, Diakonhjemmet Sykehus og Avdeling for farmasøytisk biovitenskap, Farmasøytisk institutt, Universitetet i Oslo
Forsvar av oppgaven
2010, vår
Hovedbudskap
Genetiske forskjeller iCYP2C19 er av stor betydning for farmakokinetisk variabilitet av antidepressivaene escitalopram (Cipralex®) og sertralin (Zoloft®).
Funnene kan danne grunnlag for individuell dosering av disse legemidlene for å forebygge bivirkninger og terapisvikt.
Ida Rudberg
Senter for Psykofarmakologi (tidligere Psykofarmakologisk avdeling),
Diakonhjemmet Sykehus
E-post: idarudberg@gmail.com
Last ned hele artikkelen i pdf-format.
BAKGRUNN
Depresjon er en av de vanligste psykiske lidelsene i Norge, og det anslås at om lag én av fem nordmenn vil rammes av depresjon i løpet av livet (1). Selektive serotonin reopptakshemmere (SSRI) er førstevalg ved mange former for depresjon og er derfor de mest brukte antidepressivaene her til lands. Disse legemidlene har imidlertid utilfredsstillende effekt mot depresjon hos mange av pasientene. I tillegg er plagsomme bivirkninger vanlig, for eksempel kvalme, diaré, hodepine og seksuell dysfunksjon.
Forskjeller i effekt og bivirkninger av legemidler kan skyldes at samme dose gitt til ulike pasienter gir ulik konsentrasjon av legemiddel i kroppen. Dette skyldes farmakokinetisk variabilitet, det vil si forskjeller i absorpsjon, distribusjon, metabolisme og ekskresjon av legemidlet i kroppen. Farmakokinetisk variabilitet kan håndteres ved å tilpasse legemiddeldosen til hver enkelt pasient; pasienter som får høy konsentrasjon bør få lav dose for å unngå bivirkninger, mens pasienter som får lav konsentrasjon bør få høy dose for å sikre effekt av behandlingen.
Escitalopram (Cipralex®) og sertralin (Zoloft®) er av de mest brukte SSRI-preparatene i Norge. Begge disse antidepressivaene viser stor farmakokinetisk variabilitet; opptil 40 ganger forskjell i serumkonsentrasjon etter samme dose. Individuell variasjon i legemiddelmetabolisme er en viktig årsak til farmakokinetisk variabilitet av mange legemidler. Tidligere studier har vist at både escitalopram og sertralin metaboliseres av CYP2C19-enzymet (2;3). Aktiviteten av dette enzymet er i stor grad genetisk bestemt (4). Det er imidlertid lite kjent hvordan forskjeller i CYP2C19-genet påvirker metabolismen av escitalopram og sertralin i pasienter som behandles med disse legemidlene.
Det normale CYP2C19-genet (villtypen) betegnes CYP2C19*1 (leses «CYP2C19stjerne1»). Siden 1980-tallet har det vært kjent at varianter av CYP2C19-genet gir opphav til defekt CYP2C19-aktivitet (betegnes def for defekte). Nylig ble det også identifisert en genvariant, CYP2C19*17, som innebærer økt CYP2C19-aktivitet. Totalt gir dette opphav til seks ulike CYP2C19-genotypegrupper i befolkningen;
CYP2C19*17/*17, CYP2C19*1/*17, CYP2C19*1/*1, CYP2C19*17/def, CYP2C19*1/def, CYP2C19def/def.
I Norge (kaukasiere) har ca. fem prosent av befolkningen CYP2C19*17/*17-genotypen, mens to til tre prosent har CYP2C19def/def-genotypen og er såkalte «poor metabolizers» via CYP2C19. Blant afrikanere er forekomsten av CYP2C19-genvarianter ganske lik som i kaukasiere, mens det i asiatiske populasjoner er langt høyere forekomst av defekte CYP2C19-gener (13–23 prosent er poor metabolizers), og lavere forekomst av CYP2C19*17 (5;6).
HENSIKT
Å undersøke betydningen av genetisk variasjon i CYP2C19 for farmakokinetisk variabilitet av escitalopram og sertralin i psykiatriske pasienter.
MATERIALE OG METODE
Ved Senter for Psykofarmakologi (tidligere Psykofarmakologisk avdeling) utføres serumkonsentrasjonsmålinger og CYP-genotyping av pasienter som behandles med psykofarmaka. Pasienter som var CYP-genotypet og hadde målt serumkonsentrasjon av escitalopram eller sertralin ble inkludert. Dosejustert serumkonsentrasjon (serumkonsentrasjon/døgndose i mg, omtales som «serumkonsentrasjon»), alder, kjønn, prøvetakingsbetingelser og komedikasjon ble registrert. Pasienter som ble behandlet med legemidler som er kjent å hemme eller indusere CYP2C19 ble ekskludert. Pasientene ble inndelt i seks grupper basertpå CYP2C19-genotype, og gjennomsnittlig serumkonsentrasjon i de ulike CYP2C19-genotypergruppene ble estimert og sammenliknet ved hjelp av linear mixed model analyse. Andre faktorer som potensielt kunne påvirke serumkonsentrasjonen ble undersøkt ved kovariatanalyse. CYP2C19-mediert metabolisme av escitalopram ble i tillegg studert in vitro.
RESULTATER
Sammenliknet med CYP2C19*1/*1-gruppen var gjennomsnittelig serumkonsentrasjon av escitalopram 5,7 ganger høyere i CYP2C19def/def-gruppen (p<0.001) og 42 prosent lavere i CYP2C19*17/*17-gruppen (p<0.01) (figur 1A) (7). Mellom ytterpunktene (def/def vs. *17/*17) var det ti ganger forskjell i gjennomsnittelig serumkonsentrasjon. Kvinner og bærere av defekte CYP2D6-gener hadde henholdsvis 26 prosent og 28 prosent høyere serumkonsentrasjon av escitalopram enn menn og bærere av kun funksjonelle CYP2D6-genvarianter (p<0.05). Videre indikerte in vitro-forsøk at forskjellen i serumkonsentrasjon av escitalopram mellom ulike CYP2C19-genotyper skyldes effekt på to ulike metabolismeveier; både dannelse av N-demetyl escitalopram og dannelse av escitalopram propionsyre (figur 2) (8).
For sertralin viste gruppene med defekte CYP2C19-gener signifikant høyere gjennomsnittelig serumkonsentrasjon enn CYP2C19*1/*1-gruppen (p<0.05), og for CYP2C19def/def-gruppen var effekten en 3,2 ganger høyere serumkonsentrasjon (p<0.01) (figur 1B) (9). CYP2C19*17 hadde ingen påvirkning på gjennomsnittlig serumkonsentrasjon av sertralin. Pasienter som var 70 år eller eldre hadde i gjennomsnitt 80 prosent høyere serumkonsentrasjon av sertralin enn pasienter under 70 år.
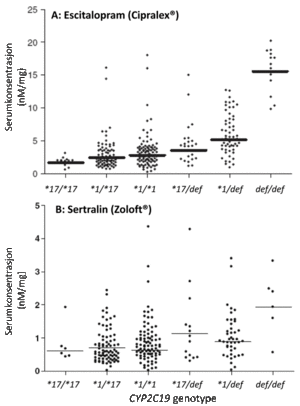
Figur 1. Dosejusterte serumkonsentrasjonsmålinger (nM/mg) av A: escitalopram (281 målinger fra 166 pasienter) og B: sertralin (238 målinger fra 121 pasienter) hos psykiatriske pasienter med ulik CYP2C19-genotype. Horisontale linjer indikerer gjennomsnittlig serumkonsentrasjon i de ulike CYP2C19-genotypegruppene. def = defekt genvariant.
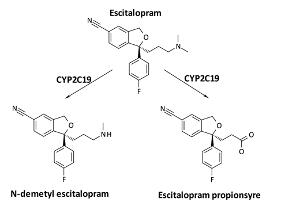
Figur 2. Kjemisk struktur av escitalopram og to metabolitter som dannes via CYP2C19; N-demetyl escitalopram og escitalopram propionsyre.
DISKUSJON
CYP2C19-genotype var av stor betydning for farmakokinetisk variabilitet av escitalopram og sertralin (7;9). Effekten av CYP2C19-genotype var størst for escitalopram, som viste ti ganger forskjell i gjennomsnittlig serumkonsentrasjon mellom ulike CYP2C19-genotyper. For både escitalopram og sertralin var effekten av defekte CYP2C19-gener større enn effekten av CYP2C19*17.
Escitalopram og sertralin er to av de mest brukte antidepressivaene i Norge, og den store forskjellen i serumkonsentrasjon mellom pasienter med ulike CYP2C19-genotyper kan være av betydning for klinisk effekt og bivirkninger av disse legemidlene. Ved bruk av standarddoser av escitalopram kan pasienter med CYP2C19*17/*17-genotypen ha økt risiko for terapisvikt, mens pasienter med defekte CYP2C19-gener kan ha økt risiko for bivirkninger ved bruk av escitalopram eller sertralin. Funnene i studien kan danne grunnlag for individuell dosering av disse legemidlene basert på CYP2C19-genotype for å forebygge bivirkninger og terapisvikt.
Både for escitalopram og sertralin var det variasjon i serumkonsentrasjon også blant pasienter med samme CYP2C19-genotype (figur 1 A og B). Dette skyldes at andre faktorer enn CYP2C19-genotype også påvirker farmakokinetikken av disse legemidlene. Kovariatanalysen viste at kjønn og CYP2D6-genetikk påvirket serumkonsentrasjonen av escitalopram, mens alder var av betydning for serumkonsentrasjonen av sertralin. Disse faktorene var imidlertid av langt mindre betydning for serumkonsentrasjonen enn pasientens CYP2C19-genotype. En annen årsak til variabilitet i serumkonsentrasjonsmålingene er at prøvene er tatt under rutinemessig oppfølging av pasientene. Dette innebærer varierende tid mellom doseinntak og prøvetaking (10–30 timer), usikker informasjon om komedikasjon samt varierende pasientetterlevelse (compliance). Det er imidlertid liten tvil om at genetisk variasjon i CYP2C19 er en hovedårsak til farmakokinetisk variabilitet av escitalopram og sertralin.
KONKLUSJON
CYP2C19-genotype er av vesentlig betydning for farmakokinetikken av escitalopram og sertralin. Effekten er størst for escitalopram hvor CYP2C19-genotype forklarer en ti ganger forskjell i serumkonsentrasjon. Funnene kan danne grunnlag for individuell dosering av sertralin og escitalopram for å forebygge bivirkninger og terapisvikt.
Referanser
- Nasjonalt folkehelseinstitutt. Psykiske lidelser i Norge: Et folkehelseperspektiv. Rapport 8, 2009.
- Herrlin K, Yasui-Furukori N, Tybring G et al. Metabolism of citalopram enantiomers in CYP2C19/CYP2D6 phenotyped panels of healthy Swedes. Br J Clin Pharmacol 2003;56:415–21.
- Wang JH, Liu ZQ, Wang W et al. Pharmacokinetics of sertraline in relation to genetic polymorphism of CYP2C19. Clin Pharmacol Ther 2001;70:42–7.
- Desta Z, Zhao X, Shin JG et al. Clinical significance of the cytochrome P450 2C19 genetic polymorphism. Clin Pharmacokinet 2002;41:913–58.
- Xie HG, Stein CM, Kim RB et al. Allelic, genotypic and phenotypic distributions of S-mephenytoin 4’-hydroxylase (CYP2C19) in healthy Caucasian populations of European descent throughout the world. Pharmacogenetics 1999;9:539–49.
- Li-Wan-Po A, Girard T, Farndon P et al. Pharmacogenetics of CYP2C19: functional and clinical implications of a new variant CYP2C19*17. Br J Clin Pharmacol 2010;69:222–30.
- Rudberg I, Mohebi B, Hermann M et al. Impact of the ultrarapid CYP2C19*17 allele on serum concentration of escitalopram in psychiatric patients. Clin Pharmacol Ther 2008;83:322–7.
- Rudberg I, Reubsaet JL, Hermann M et al. Identification of a novel CYP2C19-mediated metabolic pathway of S-citalopram in vitro. Drug Metab Dispos 2009;37:2340–8.
- Rudberg I, Hermann M, Refsum H et al. Serum concentrations of sertraline and N-desmethyl sertraline in relation to CYP2C19 genotype in psychiatric patients. Eur J Clin Pharmacol 2008;64:1181–8.
(Publisert i NFT nr. 6/2010 side 24–25.)
