Preformulering av det fotosensibiliserende stoffet TPCS2a for bruk i PCI
Marianne Lilletvedt
Farmasøytisk institutt, Universitetet i Oslo (UiO)
E-post: marianne.lilletvedt@farmasi.uio.no
BAKGRUNN OG HENSIKT
Eksisterende kreftbehandling som kirurgi, radioterapi og kjemoterapi er i mange tilfeller utilstrekkelig, og det er ønskelig å finne mer selektive behandlingsformer. Den nye, norskutviklede, patenterte teknologien fotokjemisk internalisering (PCI) gir målrettet levering av legemidler innen kreftbehandling (1). PCI-teknologien kombinerer bruk av et fotosensibiliserende stoff (PS), synlig lys og tilstedeværelse av oksygen for å levere konvensjonelle antineoplastiske legemidler til tumorvevet (figur 1). Dette fører til selektivt drap av kreftceller. Per dags dato er PCI-teknologien i klinisk utprøvning fase I/II på utvalgte grupper kreftpasienter. Videre utvikling av passende legemiddelformuleringer kan optimalisere effekten på kreftcellene og begrense bivirkningene av behandlingen.

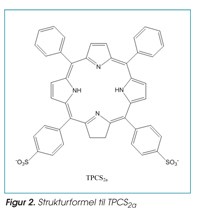
Hensikten med doktorgradsarbeidet var å foreta fysikalsk-kjemisk karakterisering av den nye forbindelsen meso-tetraphenyl chlorin disulphonate (TPCS2a; figur 2), til bruk som PS i farmasøytiske produkter utviklet for PCI innen kreftbehandling. Vandige parenterale formuleringer av TPCS2a til intravenøs eller lokal injeksjon skulle utvikles og karakteriseres. Disse formuleringene skulle gi høy selektivitet mot relevante krefttyper for å sikre optimal utnyttelse av PS og forbedret effekt av PCI teknologien (2–6).
MATERIALE OG METODER
Di(monoethanolammonium) meso-tetraphenyl chlorin disulphonate (TPCS2a) er utviklet spesielt for bruk i PCI-teknologien og ble fremskaffet av PCI Biotech AS. Pluronics ble kjøpt fra Sigma Aldrich.
Laboratorieforsøkene ble hovedsakelig utført ved Avdeling for farmasi, Farmasøytisk institutt, Universitetet i Oslo. En studie ble utført ved Avdeling for fysikk og matematikk, Universitetet for Insubria i Como, Italia (6). Spektroskopiske metoder ble brukt for eksperimentelt å bestemme interaksjoner med organiske media, dannelse av singlett oksygen, ioniseringskonstanter (pKa), distribusjonskoeffisienter (log D) og interaksjoner med Pluronics i den fysikalsk-kjemiske karakteriseringen av TPCS2a (3–6). Kapillær viskosimetri, frysepunktdepresjonsmålinger og atomisk kraftmikroskopering ble brukt for å karakterisere de vandige nanostrukturelle formuleringene av TPCS2a og Pluronics (3).
RESULTATER OG DISKUSJON
TPCS2a er utviklet spesielt for PCI-teknologien blant annet siden denne PS har høy molar absorpsjon av rødt lys som penetrerer ned i vev (~ 1 cm). Interaksjoner mellom PS og utvalgte organiske løsemidler med forskjellig polaritet, protondonor- og protonakseptoregenskaper ble vurdert spektroskopisk (5, 6). Resultatene indikerer at TPCS2a er et rigid molekyl bygget opp av konjugerte ringsystemer, som i liten grad vil interagere med omgivelsene in vitro/in vivo i grunntilstanden (det vil si i mørket) eller i eksitert tilstand (det vil si etter lysabsorpsjon). TPCS2a genererer singlett oksygen, som regnes som viktig for den selektive legemiddelfrisettingen i tumor i PCI-teknologien. pKa-verdien til TPCS2a er 3.8 (± 0.3) og log D-verdien i 1-oktanol/vann er 0.4 (± 0.4) (4). TPCS2a vil derved foreligge som anionisk fri base ved fysiologisk pH, som er den fotokjemisk aktive formen med høy amfifilisitet. Dette er avgjørende forplasseringen av PS intracellulært før fotoaktivering i PCI-teknologien.
Det er vist at TPCS2a aggregerer i vandig miljø ved farmasøytisk relevante konsentrasjoner (mg/ml), og også ved svært lave konsentrasjoner (i.v. administrasjon kan føre til alvorlige bivirkninger som emboli. I tillegg er aggregerte PS lite fotokjemisk effektive. Aggregering gjør det dermed ikke mulig å administrere TPCS2a oppløst i ren vandig løsning. Kommersielt tilgjengelige co-polymere (Pluronics) ble benyttet som solubilisatorer og nanostrukturelle legemiddelbærere i dette arbeidet (3). Den kritiske micellekonsentrasjonen (CMC) i nærvær av TPCS2a ble bestemt spektroskopisk for de fire utvalgte Pluronics L44, F68, P123 og F127 (CMC er henholdsvis 0.04, 0.05, 0.0005 og 0.001 %). TPCS2a oppløst i vann ved farmasøytiske relevante konsentrasjoner (≥10 mg/ml) gir prøver med høy viskositet på grunn av aggregering og nettverksdannelse. Pluronickonsentrasjonene som var nødvendige for å bryte ned nettverket av TPCS2a og nå et akseptabelt viskositetsnivå var flere ganger de respektive CMC-verdiene (henholdsvis 15, 12, 400 og 300 ganger CMC for L44, F68, P123 og F127). Utvalgte prøver ble visualisert ved bruk av atomisk kraftmikroskop, og bildene viste at interaksjoner finner sted mellom nanobærerne (Pluronics) og TPCS2a. Strukturene som ble dannet kan være polymere miceller med solubilisert TPCS2a, eller aggregater av TPCS2a med Pluronic adsorbert til overflaten (3).
Formuleringer til intravenøs injeksjon bør være isotone. Isotoniregulatorer (5 % glukose- eller 0.9 % natriumkloridløsninger) påvirket imidlertid viskositeten til prøvene i stor grad. De isotone prøvene som inneholdt TPCS2a (10 mg/ml), Pluronic (0.6 %) og isoton glukose- eller NaCl-løsning var mer viskøse enn kun de vandige løsningene av TPCS2a (10 mg/ml) og Pluronic (0.6 %). Effektene som forårsaker dette fenomenet er ikke endelig bestemt, men ser ut til å ha sammenheng med molekylstrukturen til TPCS2a, molekylær ladning og asymmetri. Dette er en utfordring i videre produktutvikling, siden TPCS2a-Pluronicsformuleringene også vil aggregere i nærvær av salter og glukose i blodsirkulasjonen og derved ikke er egnet til intravenøs administrering (3). Formuleringene kan imidlertid være anvendbare for alternative administrasjonsruter inkludert lokal administrering for selektiv kreftterapi. Videre formuleringsarbeid vil bli utført. Bruk av optimale farmasøytiske formuleringer vil medføre at PS utnyttes best mulig, kan gis til pasienten på ønsket måte, at effekten av PCI-teknologien blir forbedret, og at et farmasøytisk preparat kan produseres på en enkel og sikker måte.
KONKLUSJON
Preformuleringsarbeidet med TPCS2a ga grunnleggende kunnskap om egenskapene til dette fotosensibiliserende stoffet, som kan benyttes i det videre formuleringsarbeidet ved bruk av denne forbindelsen i PCI-teknologi rettet mot kreftbehandling. Legemiddelet er vanskelig å formulere, men bruk av de nanostrukturelle legemiddelbærerne Pluronics kan benyttes til å solubilisere TPCS2a i vandige formuleringer til topikal administrasjon eller lokal injeksjon. Flytegenskapene til disse formuleringene er svært følsomme for tilsetningsstoffer og omgivelser in vitro/in vivo, og dette må studeres videre. Styring av flytegenskaper kan imidlertid utnyttes iutvikling av produkter, for eksempel til lokal levering av legemiddelet til pasient (injeksjon i svulst eller applikasjon på svulstoverflate).
Referanser
- Selbo PK et al. Photochemical internalization provides time- and space-controlled endolysosomal escape of therapeutic molecules. J Control Release 2010; 148: 2–12.
- Lilletvedt M. Pharmaceutical preformulation of the amphiphilic photosensitizer TPCS2a for application in photochemical internalization (PCI). Doktoravhandling. Oslo: Faculty of Mathematics and Natural Sciences, University of Oslo, 2011.
- Lilletvedt M et al. Solubilization of the novel anionic amphiphilic photosensitizer TPCS2a by nonionic Pluronic block copolymers. Eur J Pharm Sci 2011; 43: 180–187.
- Lilletvedt M et al. Evaluation of physicochemical properties and aggregation of the photosensitizers TPCS2a and TPPS2a in aqueous media. Pharmazie 2011; 66: 325–333.
- Lilletvedt M et al. Physicochemical characterization of the photosensitizers TPCS2a and TPPS2a 1.Spectroscopic evaluation of drug-solvent interactions. Pharmazie 2010; 65: 588–595.
- Lilletvedt M et al. Time-domain evaluation of drug-solvent interactions of the photosensitizers TPCS2a and TPPS2a as part of physicochemical characterization. J Photochem Photobiol A: Chem 2010; 214: 40–47.
(Publisert i NFT nr. 1/2012 side 32–33.)
