Bisfosfonatrelatert kjevebensnekrose; europeiske og norske erfaringer
Sammendrag
Hensikt
Kjevebensnekrose er en sjelden, men alvorlig og terapiresistent bivirkning ved bisfosfonatbehandling. Hensikten med arbeidet er å formidle oppsummeringer og konklusjonene fra europeiske legemiddelmyndigheters eksperter og å presentere omfanget av bisfosfonatrelatert kjevebensnekrose rapportert i Norge og verden.
Materiale og metoder
Artikkelen er basert på europeiske legemiddelmyndigheters ekspertmøte i mars 2009, i tillegg til artikler fra et ikke-systematisk søk i PubMed. Bivirkningsdata ble skaffet fra Statens legemiddelverk og Verdens helseorganisasjon per 16. november 2010.
Resultater
Ekspertenes vurdering var at biologisk potens, administrasjonsrute og dose (enkel/kumulativ) av bisfosfonater er viktige risikofaktorer for bisfosfonatrelatert kjevebensnekrose. Dentale prosedyrer som tannekstraksjon og rotfylling, kjevebenkirurgi, intraorale traumer, preeksisterende dental og periodontal sykdom, glukokortikoidbruk, malign sykdom, stråling og genetiske faktorer er antakelig avgjørende predisponerende elementer.
Per 16. november 2010 var 52 bisfosfonatrelatert kjevebensnekrose meldt til den norske bivirkningsdatabasen; 34 etter behandling med intravenøst zoledronat og 18 etter peroralt alendronat, mens på verdensbasis var det totalt 1954 tilfeller rapportert.
Konklusjon
Tannhelsen bør spesielt vurderes hos kreftpasienter tiltenkt intravenøs administrasjon av bisfosfonater, men også hos andre pasienter med dårlig tannstatus. Dentale prosedyrer bør gjøres så konservativt som mulig hos risikopasienter. Det er viktig med god munnhygiene og jevnlig tannhelsesjekk. Tannlege/lege bør kontaktes ved uvanlige symptomer i munnhulen (smerter, hevelse og løse tenner).
Norsk Farmaceutisk Tidsskrift 2012; 1: 26–30.
Hovedbudskap
Kjevebensnekrose er en sjelden, men alvorlig og terapiresistent bivirkning ved bisfosfonatbehandling.
Tannhelsen bør vurderes spesielt før intravenøs bisfosfonat administrasjon og generelt hos alle pasienter med dårlig tannstatus tiltenkt bisfosfonatbehandling. Dentale/orale prosedyrer bør gjøres så konservativt som mulig hos risikopasienter.
Tannlege/lege bør kontaktes dersom noe uvanlig i munnhulen som smerte, hevelse og løse tenner merkes hos bisfosfonatbrukere.
Review article, Summary
Bisphosphonate related osteonecrosis of jaw; European and Norwegian experiences
Background
Osteonecrosis of jaw is a rare but serious and therapy resistant side effect of bisphosphonate treatment and is often called bisphosphonate-related osteonecrosis of jaw (BONJ). The aim of this paper is to summarize the conclusions and recommendations of the expert meeting by the European Medicines Agency and to present reported cases to the Norwegian Medicines Agency and to the World Health Organization.
Material and methods
This article is based on the expert meeting which was held in March 2009 and articles from a non-systematic search in PubMed. BONJ reports were obtained from the Norwegian Medicines Agency as of mid-November 2010.
Results
Biological potency, administration route and dose (single/cumulative) of bisphosphonates were considered to be important risk factors for BONJ by the experts. Dental/periodontal disease, dental procedures, jaw bone surgery, glucocorticoid treatment, malignant disease, radiation and genetic factors are probably predisposing elements for BONJ. As of mid-November 2010 were 52 BONJs reported to the Norwegian Medicines Agency, of which 34 after intravenous zoledronate treatment and 18 after oral alendronate administration while on world basis 1954 cases were reported.
Conclusion
Dental health should in particular be checked among cancer patients intended intravenous administration of bisphosphonates but also in other patients with poor dental status. All dental procedures should be made as conservatively as possible in patients at risk. Good oral hygiene and frequent dental checks are important. Dentist/physician should be contacted in case of unusual symptoms such as oral pain, swelling and loose teeth).
Norsk Farmaceutisk Tidsskrift 2012; 1: 26–30.
Last ned hele artikkelen i pdf-format.
BAKGRUNN
Norge er på verdenstoppen i antall lårhalsbrudd og benskjørhet, sett i forhold til folketallet. Dette medfører at vi er storforbrukere av bisfosfonater hovedsakelig for indikasjonen postmenopausal osteoporose. I tillegg brukes bisfosfonater hos kreftpasienter med benmetastaser og/eller hyperkalsemi.
Kjevebensnekrose kan oppstå etter behandling med bisfosfonater. Dette kalles bisfosfonatrelatert kjevebensnekrose (BONJ, «bisphosphonate related osteonecrosis of jaw»). Det er etter hvert enighet om at BONJ kan defineres som «tilstedeværelse av eksponert ben i underkjeven og/eller overkjeven som ikke lar seg tilhele i løpet av åtte uker hos pasient som bruker eller har brukt bisfosfonater». Stråling av kjevene skal være utelukket. BONJ er et terapiresistent klinisk syndrom hvor patofysiologien ikke er klarlagt. Europeiske legemiddelmyndigheters (EMA) vitenskapelige komité (Committee for Human Medicinal Products, CHMP) og dens arbeidsgruppe for legemiddelovervåking (Pharmacovigilance Working Party, PhVWP), arrangerte et ekspertmøte i mars 2009. Målsettingen med møtet var å sette fokus på følgende tema; I) definisjon av BONJ og diagnosekriterier, II) underliggende patofysiologi, III) risikostratifisering mellom produktene og pasientpopulasjonene, og IV) risikoreduserende tiltak. I september 2009 publiserte EMA en rapport fra møtet (1), og Statens legemiddelverk informerte om dette på sin hjemmeside (2). Hensikten med denne oversikten er å presentere omfanget av BONJ rapportert i Norge og å formidle oppsummeringer og konklusjonene fra europeiske legemiddelmyndigheters eksperter.
MATERIALE OG METODER
Artikkelen er basert på ekspertmøtet og artikler fra et ikke-systematisk søk i PubMed. Bivirkningsdata ble skaffet fra Statens legemiddelverk og ble gjort ved søk både i Legemiddelverkets bivirkningsdatabase (for Norge) og i Verdens helseorganisasjon (WHO)-databasen (internasjonalt) per 16. november 2010. EMAs vitenskapelige komité og dens arbeidsgruppe for legemiddelovervåking arrangerte et ekspertmøte i mars 2009. Ekspertgruppen var bredt sammensatt av oral/maxillofacial-kirurger, klinikere, forskere og representanter fra legemiddelmyndighetene i flere EU/EØS-land inkludert Norge. EMA har utarbeidet en utredningsrapport som er offentliggjort. I september 2009 publiserte EMA en rapport fra møtet (1), og Statens legemiddelverk informerte om dette på sin hjemmeside (2).
RESULTATER
Virkningsmekanisme, struktur og potens
Det er viktig å se på bisfosfonatenes struktur, aktivitet og farmakodynamiske mekanismer for å forstå BONJ bedre. En nylig publisert oversiktartikkel av Drake et al. (3) gir en god oversikt over bisfosfonatenes virkningsmekanismer, kliniske bruk og bivirkninger.
Bisfosfonater deles i to grupper; ikke-nitrogenholdige og nitrogenholdige. Modersubstansen for alle er uorganisk pyrofosfat (figur 1a). Bisfosfonater hemmer osteoklastenes aktivitet. Osteoklaster er celler som først og fremst har som oppgave å resorbere bensubstans. Bisfosfonater kan dermed til en viss grad rette opp eventuell ubalanse mellom osteoklast-mediert bennedbryting og osteoblast-mediert benoppbygging.
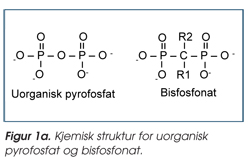
Ikke-nitrogenholdige bisfosfonater inkorporeres som falske nukleotider i adenosintrifosfat (ATP). Falske ikke-hydrolyserbare ATP-analoger antas å være toksisk for osteoklaster og forårsaker programmert celledød (apoptose). Nitrogenholdige bisfosfonater virker via helt andre mekanismer. De forårsaker apoptose av osteoklaster ved å hemme farnesylpyrofosfatsyntase, et sentral regulatorisk enzym i mevalonsyremetabolismen. Dette enzymet er involvert i produksjon av steroler, inkludert kolesterol. I tillegg forårsaker de nitrogenholdige bisfosfonatene post-translasjonelle proteinmodifikasjoner av type isoprenylering. Dette affiserer viktige guanusintrifosfat-bindende proteiner som Rab, Rac og Rho og dermed viktige funksjoner i osteoklastene. Det er også antatt at bisfosfonater kan redusere apoptose i osteoblaster og osteocytter.
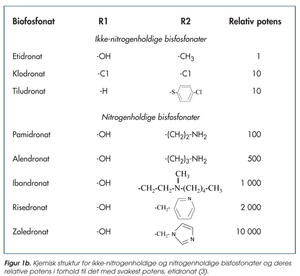
Potensen og den kliniske effekten av bisfosfonater er sannsynligvis relatert til stoffenes mineralbindende evne og evne til å hemme enzymet farnesylpyrofosfatsyntase (4). Figur 1b viser bisfosfonatenes relative potens i forhold til det med svakest potens, etidronat (3). Det er estimert at alendronat har en biologisk halveringstid på ca. 10 år etter en enkel intravenøst administrasjon (5). Det foregår fortsatt diskusjoner om den biologiske halveringstiden til de forskjellige bisfosfonater. Dette viser seg å være teknisk utfordrende siden måling av disse stoffene i urin og serum ikke er så lett på grunn av lave konsentrasjoner, ikke minst fordi stoffene i stor grad inkorporeres i beinvev og blir værende der.
BONJ diagnosekriterier
Kjevebensnekrose kan inndeles i tre stadier hvor stadium én indikerer nekrotisk ben hos asymptomatiske pasienter uten tegn til infeksjon. I stadium to forekommer også smerte og infeksjon. Pasienter i stadium tre har i tillegg én eller flere av følgende symptomer: ekspansjon av nekrosen utover alveolart ben resulterende i patologisk fraktur, ekstraoral fistul, oral-antral/oral-nasal forbindelse eller osteolyse gjennom underkjeven eller sinusgulvet. Man kan også definere et stadium null hos pasienter med ikke-spesifikk smerte uten eksponert ben. Røntgenbilder i stadium null kan gi informasjon som gir mistanke om mulig kjevebensnekrose under utvikling. Scintigrafi eller PET-bilde kan også bidra til å identifisere dette stadiet, men det er fortsatt ikke klarlagt hvor nyttig disse metodene er.
Underliggende patofysiologi
Assosiasjon mellom bruk av bisfosfonat og BONJ ble først påvist i 2003 (6). Kausal sammenheng mellom bifosfonatbruk og kjevebensnekrose er fortsatt ikke dokumentert, men det er mye data som viser en tidsmessig sammenheng mellom bisfosfonatbruk og kjevebensnekrose.
Man har spekulert på hvorfor bisfosfonater forårsaker osteonekrose i kjeven og ikke i andre ben. Det kan tenkes at dette henger sammen med en høy blodforsyning til kjevene, kjevenes struktur, funksjon, arbeidsbelastning og mikrobiologi (7, 8). Det er stor sannsynlighet for at det er en multifaktoriell årsak til BONJ. Flere nylig publiserte arbeider har diskutert mulige mekanismer, blant annet immunmodulering, infeksjon, høy benomsetning («turnover»), forstyrrelser i angiogenesen, toksiske effekter i bløtvev eller direkte i ben (9–11). Det er også foreslått andre mekanismer som hypokalsemi og sekundær hyperparatyroidisme (12). Forstyrrelser i likevekten mellom osteoklast- og osteoblast-aktivitet (13),cancermetastaser og synergiske effekter med andre farmaka som kjemoterapeutika og kortikosterioder diskuteres som mulige mekanismer. Genetiske faktorer kan ha betydning og matriksmetalloproteinase 2 og Rs 1934951 polymorfismen i cytokrom P-450-enzymet CYP2C8 er foreslått som kandidat-gener (14, 15).
Risikostratifisering basert på indikasjon, produkt og pasientpopulasjon
Kreftpasienter som får bisfosfonater intravenøst er ansett for å ha størst risiko for å få BONJ (11). Den kumulative insidensen er anslått til mellom 0,8 % og 12 % (16), mens blant osteoporosepasienter og pasienter med Pagets sykdom som får bisfosfonater peroralt, er insidens av BONJ lav og anslått til å ligge mellom 0,0004 % og 0,06 %. Risiko hos pasienter med osteoporose som får bisfosfonater intravenøst er ikke kjent, men antas å være betydelig lavere enn hos kreftpasienter som mottar flere intravenøs administrasjoner i løpet av kort tid. En nylig publisert studie (17) viste at BONJ oppsto hos 4 % av pasienter som tok alendronat og gjennomgikk invasive tannprosedyrer. Dette er en viktig studie som bør følges opp. Den hyppige forekomst av BONJ i denne studien kan trolig tilskrives seleksjon av høyrisikopasienter.
Det er en felles forståelse av at indikasjonen for bruk av bisfosfonater ikke er den faktoren som har størst betydning for utviklingen av BONJ.
Bifosfonatens biologiske potens, administrasjonsmåte, enkeltdose, hvilken hastighet preparatet gis med (for intravenøs bruk) og den kumulative dosen er sannsynligvis viktigere risikofaktorer. Én årlig engangsdose ved behandling av postmenopausal osteoporose er godkjent indikasjon for zoledronat (preparatet Aclasta i Norge). En enkelt årlig dose zoledronat ved behandling av osteoporose gir sannsynligvis færre tilfeller av BONJ enn multiple doser zoledronat hos kreftpasienter. EMA anser det likevel som viktig å overvåke nøye intravenøs bruk av bisfosfonater hos ikke-kreftpasienter. Man er imidlertid klar over at det er en risiko for at den lave frekvensen av BONJ hos osteoporose-pasienter ved bruk av peroralt bisfosfonat i fremtiden kan bli økende hos eldre kvinner som tidligere har brukt bisfosfonater i lang tid. I en nylig publisert studie har man undersøkt relasjonen mellom den kumulative dosen og latenstiden før BONJ oppstår («time to event») med zoledronat, pamidronat og orale bisfosfonater (18). Studien er en sammenstilling av i alt 71 kasusserier utført etter 2003. «Time to event» etter zoledronat ble estimert til 1,8 år (minimumstid 10 måneder); etter pamidronat 2,8 år (minimumstid 1,5 år) og etter orale bisfosfonater 4,6 år (minimumstid 3 år). Forfatterne påpeker at invasive dentale prosedyrer, høy alder, revmatisme, diabetes, kortikosteroidbruk og vitamin D-mangel er blant de viktigste medvirkende årsaker til BONJ og er avgjørende for den tiden det tar til BONJ oppstår.
Forekomst av BONJ og bruk av bisfosfonater i Norge
Tall fra Reseptregisteret fra 2009 viser at henholdsvis 46 533 kvinner og 5 966 menn hentet ut resept på alendronat, mens henholdsvis 710 og 125 kvinner og menn hentet ut resept på zoledronat (19). Det antas at de fleste som får zoledronat med kreftdiagnose, får denne behandlingen på sykehus og er derfor ikke med i tallene fra Reseptregisteret. Tall fra grossiststatistikken viser at det ble solgt henholdsvis 9,05 og 0,01 definerte døgndoser (DDD)/1000 innbyggere/dag for alendronat og zoledronat.
Søk påMedDRA («the Medical Dictionary for Regulatory Activities») terminologi «osteonecrosis of jaw» i den norske bivirkningsdatabasen ved Statens legemiddelverk per 16. november 2010 gav 52 tilfeller av bisfosfonatindusert ONJ (tabell 1). Alendronat tas peroralt ved postmenopausal osteoporose og zoledronat intravenøst ved maligne tilstander. Intravenøst zoledronat gitt en gang i året med indikasjon osteoporose ble først godkjent i september 2005 (godkjent preparat i Norge er Aclasta).

Registrert BONJ ved Verdens helseorganisasjon (WHO)
Søk på MedDRA terminologi «osteonecrosis of jaw» og bisfosfonater og bifosfonatkombinasjoner ved WHOs bivirkningsdatabase per 16. november 2010 gav 1954 tilfeller av BONJ. Av dette var 1145 tilfeller relatert til zoledronat, 281 til alendronate, 280 til pamidronate, 123 til ibandronat, 58 til risedronat og resten til andre bisfosfonater. Registrert tall for MedDRA terminologi «osteonecrosis» og bisfosfonater og bifosfonatkombinasjoner er for øvrig mye høyere (8824) for samme tidsperiode. Det kan ikke utelukkes at en del av disse også kan dreie seg om BONJ.
WHO presiserer at denne informasjonen ikke sier noe om opprinnelse, årsakssammenheng eller ansvarlig farmasøytisk produkt for bivirkningen og at denne informasjonen ikke representerer WHOs oppfatning.
DISKUSJON
Kjevebensnekrose er en sjelden, men alvorlig og terapiresistent bivirkning ved bisfosfonatbehandling som har størst forekomst ved intravenøst administrasjon hos kreftpasienter. Årsaken er sannsynligvis multifaktoriell og biologisk potens av den enkelte bisfosfonat, administrasjonsrute og dose (enkel/kumulativ) av bisfosfonater er viktige risikofaktorer. Det var rapportert 52 BONJ til den norske bivirkningsdatabasen per medio november 2010.
Risikoreduserende tiltak – råd fra ekspertgruppen
Retrospektive studier indikerer at preventive og konservative tannhelsetiltak kan redusere risiko for BONJ. I en studie (20) ble forekomsten av ONJ hos pasienter med solide tumores redusert fra 3,2 % i kontrollgruppen til 1,3 % hos pasienter som fikk tannhelsessjekk (og ortopantomografi) før behandling med henholdsvis pamidronat (62 %), zoledronat (25 %), pamidronat etterfulgt av zoledronat (8 %) og klodronat (5 %).
Den biologiske potensen, administrasjonsmåten og den kumulative dosen er sentrale faktorer assosiert med utvikling av BONJ. Ved intravenøs bisfosfonatbruk hos kreftpasienter øker risiko for BONJ med økende doser og lengde/frekvens av behandling. En retrospektiv studie hos 106 pasienter med multiple myelomer viste åtte ganger risikoreduksjon når frekvens av behandlingen med intravenøs zoledronat/pamidronat etter første året ble redusert fra månedlige doser til dosering hver tredje måned. Risikoen for BONJ kan derfor trolig reduseres ved å redusere dose, administrasjonsfrekvens og behandlingsvarighet uten at det går på bekostning av den kliniske nytten, Corso et al. (21).
For perorale bisfosfonater er det ennå ingen holdepunkter for at forandring av doseringsmønster/-intervall kan redusere insidensen av BONJ. Videre studier hos denne gruppen av pasienter er nødvendig når det gjelder langtidssikkerhet.
I en litteraturoversikt (22) forslås det at seponering av bisfosfonater før elektiv tannekstraksjon kan redusere risiko, mens andre ikke deler denne oppfatningen, noe som begrunnes med den langebiologiske halveringstiden av bisfosfonater (23, 24).
Rådene til helsepersonell og pasientene vil i korte trekk være følgende: Tannhelsen bør vurderes før behandling med bisfosfonater settes i gang. Dette er viktigst hos kreftpasienter som skal ha intravenøs administrasjon av bisfosfonater, men også hos pasienter med generelt dårlig tannstatus som skal ha peroral behandling med bisfosfonater. Aktsomhet må utvises hos pasienter som bruker bisfosfonater i forbindelse med større inngrep som tannekstraksjon eller kjeveoperasjoner. Behandlingen bør utføres så konservativt som mulig. Pasienter som tar bisfosfonater må være nøye med munnhygiene, ha jevnlig tannhelsesjekk og kontakte tannlege/ lege hvis de merker noe uvanlig i munnhulen som smerte, hevelse og løse tenner.
VIDERE FORSKNING – råd fra ekspertgruppen
Prekliniske og basale studier nødvendige
Dyremodeller som er egnet til studier av lokal vaskularisering, anatomi, ben-metabolisme, mikrotraumer og immunologiske mekanismer for BONJ er ansett som viktige, således studier som evaluerer toksiske konsentrasjoner og akkumulering av bisfosfonater i diverse celletyper som osteocytter og osteoblaster. Det er også behov for farmakokinetiske studier som belyser halveringstid og akkumulering av bisfosfonater i kjeveben og andre knokler, og hvordan akkumuleringen affiseres av ulike injeksjonshastigheter.
Kliniske og epidemiologiske prospektive studier
Mange av ekspertene som deltok på møtet i EMA etterlyste opprettelse av en pan-europeisk database som samler alle tilfeller av kjevebensnekrose. Dette vil kunne danne grunnlag for økt kunnskap om bakgrunnsinsidens av kjevebensnekrose, insidens av medikamentrelatert kjevebensnekrose, kunnskap om tid til symptomdebut, indikasjon, risikofaktorer og genetiske faktorer. En slik database vil være av stor betydning for å kunne evaluere effekten av eventuelle tiltak som alternative doseringsregimer og tannundersøkelser før administrasjon av bisfosfonater. Det er også behov for flere prospektive kontrollerte studier, «case-control» studier, farmakogenetiske og farmakoepidemiologiske studier.
KONKLUSJON
Kreftpasienter som får bisfosfonater intravenøst er ansett for å ha størst risiko for å få BONJ, mens hos osteoporosepasienter og pasienter med Pagets sykdom som får bisfosfonater peroralt er forekomsten av BONJ lav. Biologiske potens, intravenøs administrasjon, dose (enkel/kumulativ) av bisfosfonater er viktige risikofaktorer for BONJ. Invasive dentale inngrep kan øke risikoen for BONJ. Tannhelsen bør vurderes før behandling med bisfosfonater startes, spesielt før intravenøs administrasjon hos kreftpasienter, men dette er også viktig hos andre pasienter med generell dårlig tannstatus uansett administrasjonsvei og indikasjon. Dentale/orale prosedyrer bør gjøres så konservativt som mulig hos risikopasienter. Pasienter som tar bisfosfonater må være nøye med munnhygiene, ha jevnlig tannhelsesjekk og kontakte tannlege/lege hvis de merker noe uvanlig i munnhulen som smerte, hevelse og løse tenner.
Stor takk til Statens legemiddelverk ved seniorrådgiver Hilde Samdal for søkene i bivirkningsdatabasene og seniorrådgiver Ingebjørg Buajordet for nyttige kommentarer på manuskriptet. Likeledes stor takk til professor dr.med. Odd Brørs ved Oslo universitetssykehus for kommentarer på manuskriptet.
Oppgitte interessekonflikter: Ingen
Litteratur
- CHMP assessment report on bisphosphonates and osteonecrosis of the jaw. www.ema.europa.eu/docs/en_GB/document_library/Report/2010/01/WC500051428.pdf
- Kjevenekrose og bisfosfonater. www.legemiddelverket.no/templates/InterPage____80923.aspx
- Drake MT, Clarke BL, Khosla S. Bisphosphonates: mechanism of action and role in clinical practice. Mayo Clin Proc 2008; 83: 1032–45.
- Russell RG, Watts NB, Ebetino FH et al. Mechanisms of action of bisphosphonates: similarities and differences and their potential influence on clinical efficacy. Osteoporos Int 2008; 19: 733–59.
- Khan SA, Kanis JA, Vasikaran S et al. Elimination and biochemical responses to intravenous alendronate in postmenopausal osteoporosis. J Bone Miner Res 1997; 12: 1700–7.
- Marx RE. Pamidronate (Aredia) and zoledronate (Zometa) induced avascular necrosis of the jaws: a growing epidemic. J Oral Maxillofac Surg 2003; 61: 1115–7.
- Adamo V, Caristi N, Sacca MM et al. Current knowledge and future directions on bisphosphonate-related osteonecrosis of the jaw in cancer patients. Expert Opin Pharmacother 2008; 9: 1351–61.
- Marx RE, Sawatari Y, Fortin M et al. Bisphosphonate-induced exposed bone (osteonecrosis/osteopetrosis) of the jaws: risk factors, recognition, prevention, and treatment. J Oral Maxillofac Surg 2005; 63: 1567–75.
- Novince CM, Ward BB, McCauley LK. Osteonecrosis of the jaw: an update and review of recommendations. Cells Tissues Organs 2009; 189: 275–83.
- Reid IR. Osteonecrosis of the jaw: who gets it, and why? Bone 2009; 44: 4–10.
- Silverman SL, Landesberg R. Osteonecrosis of the jaw and the role of bisphosphonates: a critical review. Am J Med 2009; 122: S33–45.
- Ardine M, Generali D, Donadio M et al. Could the long-term persistence of low serum calcium levels and high serum parathyroid hormone levels during bisphosphonate treatment predispose metastatic breast cancer patients to undergo osteonecrosis of the jaw? Ann Oncol 2006; 17: 1336–7.
- Sarin J, DeRossi SS, Akintoye SO. Updates on bisphosphonates and potential pathobiology of bisphosphonate-induced jaw osteonecrosis. Oral Dis 2008; 14: 277–85.
- Lehrer S, Montazem A, Ramanathan L et al. Bisphosphonate-induced osteonecrosis of the jaws, bone markers, and a hypothesized candidate gene. J Oral Maxillofac Surg 2009; 67: 159–61.
- Sarasquete ME, Garcia-Sanz R, Marin L et al. Bisphosphonate-related osteonecrosis of the jaw is associated with polymorphisms of the cytochrome P450 CYP2C8 in multiple myeloma: a genome-wide single nucleotide polymorphism analysis. Blood 2008; 112: 2709–12.
- American Association of Oral and Maxillofacial Surgeons position paper on bisphosphonate-related osteonecrosis of the jaws. J Oral Maxillofac Surg 2007; 65: 369–76.
- Sedghizadeh PP, Stanley K, Caligiuri M et al. Oral bisphosphonate use and the prevalence of osteonecrosis of the jaw: an institutional inquiry. J Am Dent Assoc 2009; 140: 61–6.
- Palaska PK, Cartsos V, Zavras AI. Bisphosphonates and time to osteonecrosis development. Oncologist 2009; 14: 1154–66.
- Reseptregisteret www.reseptregisteret.no/Prevalens.aspx
- Ripamonti CI, Maniezzo M, Campa T et al. Decreased occurrence of osteonecrosis of the jaw after implementation of dental preventive measures in solid tumour patients with bone metastases treated with bisphosphonates. The experience of the National Cancer Institute of Milan. Ann Oncol 2009; 20: 137–45.
- Corso A, Varettoni M, Zappasodi P et al. A different schedule of zoledronic acid can reduce the risk of the osteonecrosis of the jaw in patients with multiple myeloma. Leukemia 2007; 21: 1545–8.
- Khosla S, Burr D, Cauley J et al.Bisphosphonate-associated osteonecrosis of the jaw: report of a task force of the American Society for Bone and Mineral Research. J Bone Miner Res 2007; 22: 1479–91.
- King AE, Umland EM. Osteonecrosis of the jaw in patients receiving intravenous or oral bisphosphonates. Pharmacotherapy 2008; 28: 667–77.
- Woo SB, Hellstein JW, Kalmar JR. Narrative [corrected] review: bisphosphonates and osteonecrosis of the jaws. Ann Intern Med 2006; 144: 753–61.
Manuskriptet ble mottatt 6. september 2011 og godkjent 10. november 2011.
Norsk Farmaceutisk Tidsskrift 2012; 1: 26–30.
