Ny genteknologi tilbud og etterspørsel
Tekst: Johan Holst, seniorforsker, Nasjonalt folkehelseinstitutt,
Oslo og Siena
I den senere tid har det gått svært kort tid fra et vitenskapelig gjennombrudd presenteres på internasjonale konferanser og i prestisjetunge tidsskrifter, til at en tilpasset anvendelse av «gjennombruddet» reklameres for i dagspresse. Videre blir det aktuelle tilbudet gjort tilgjengelig via internett og postordre for kunder som kan, og er villige til å betale. Eksempler på slike tilbud er identifisering av barnets kjønn seks uker etter befruktning («The Pink or Blue Test»); lage kloninger av kjæledyr; finne ut hvor i verden ens egen slekt stammer fra og hvilke sykdommer man er disponert for.

Litt om teknikk og begreper
Gener og arvematerialets sammensetning samt struktur har vært betydelige utfordringer for vitenskapen siden Gregor Mendel og Charles Darwin på slutten av 1800-tallet. Av nøkkelbegivenheter fra vår relativt nære fortid kan nevnes James Watson, Francis Crick og Maurice Wilkins med oppklaringen av den dobbelte spiralstrukturen til DNA (1953). Vi bør også minnes gjennombrudd som DNA-sekvensering (Fred Sanger i 1975), polymerase kjedereaksjon («PCR» av Kary Mullins i 1984) og den formidable innsatsen knyttet til «The Human Genome Project» fra 1990 til 2001/ca. 2004. I 2007 ble så for første gang et enkelt menneskes komplette genom presentert (J. Craig Venter).
PCR-metoden
PCR-metoden kan betegnes som «arbeidshesten» i all genteknologi. Denne teknikken baserer seg på et varmestabilt enzym (DNA-polymerase fra en bakterie som finnes naturlig i varme kilder) som setter sammen byggesteinene (nucleosider) til DNA-kjeder ved 72 oC. Effektiviteten er enorm; 32 kopier av en DNA-tråd etter fem runder og over en milliard etter 30 runder (regn da ut hvor mange kopier det blir om man starter med ca. 80 000, som er en ordinær konsentrasjon i en prøve man ønsker å forsterke). Når den aktuelle DNA-biten er oppformert tilstrekkelig kan den analyseres (sekvenseres) og eventuelt settes inn i en bakterie, gjærsopp eller en annen organisme for å uttrykke genproduktet (proteinet).
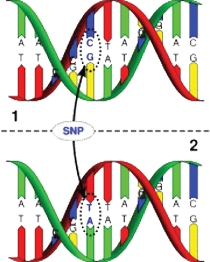
Figur 1. SNPs («Single Nucleotide Polymorphisms») er et akronym flere farmasøyter må få et forhold til. Kopieringsfeil skjer og kan gi endringer i egenskaper. Her finnes nøkkelen til individualisert medisin/terapi («Personalized Medicine»)!
STRs og SNPs
Av andre begrep og forkortelser det er verdt å kjenne til er STRs («Short Tandem Repeats») og SNPs («Single Nucleotide Polymorphisms»). STR brukes blant annet i rettsmedisin for å identifisere et individ. Altså et genetisk «fingeravtrykk», basert på helt unike mønstre som oppstår ved kopieringsfeil av repeterende sekvenser som for eksempel AATGAATGAATG (3 gangers repetisjon av «tandem-motivet»; alternativt 4 til 7 ganger) i det området av DNA som ikke koder for proteiner. For farmasøyter er imidlertid SNPs betydelig viktigere, da det er her nøkkelen til individualisert medisin/terapi («Personalized Medicine») ligger. Grunnlaget for dette er kopieringsfeil i funksjonelle gener (altså de som koder for proteiner). Feilen består i at en «bokstav» (nukleotidet, eller purin-/pyrimidin basen) byttes ut med en annen. For eksempel gir A istedenfor G i GAT en helt annen aminosyre (tripletten leses da som AAT), se figur 1. Det aktuelle proteinet får da trolig en ganske annen funksjonalitet. Mulige effekter kan være lavere nedbrytningshastighet av legemidler, disposisjon for spesielle bivirkninger og økt risiko, eller mottakelighet for bestemte sykdommer.

PCR («Polymerase Chain Reaction») er «arbeidshesten» i moderne genteknologi. «Enkelt, raskt og renslig ...» Foto: Wikipedia
Tilbud via internett
SNPs er også sentralt når det gjelder såkalt screening av individers genom for identifisering av disposisjon eller økt sannsynlighet for utvikling av bestemte sykdommer senere i livet (som enkelte former for kreft, diabetes type 1 og fedme). Tilbudene om individuell genetisk analyse og rådgivning har fått et betydelig omfang det siste året. Firmaet «23and Me», basert i California, går høyt på banen og hevder at de demokratiserer individuell genetikk (altså ingen reguleringer eller medisinske autoriteter mellom kunden og firmaet). Det islandske «deCODEme» bruker blant annet utsagnet «A hypocondriac meets deCODEme and comes out eating appels» for å inngi tillit og presentere sitt syn på verdien av denne typen gentesting. Eller for å bruke deres egen formulering: «Discover what a deCODEme DNA test can tell you about improving your health and lowering the risks of developing genetic diseases». Har man ikke direkte firmatilknytning fortoner vel mye av denne typen utsagn seg som et betydelig oversalg. Det kan nok være spennende og preget av nyhetens interesse å få sine genetiske anlegg undersøkt. Enkelte ganger trolig også nyttig, men rådene man får er jo egentlig de klassiske tre: «Ikke røyk, mosjoner og spis mindre!»
Den pågående ekspansjonen og kommersialiseringen av de ulike genetiske tilbud har vokst frem i kjølvannet av «The Human Genome Project». Dette USA-baserte «månelandingsprosjektet» tok ca. 13 år,involverte over 20 ulike institusjoner fra mange ulike land og kostet mer enn 15 milliarder kroner. Helt siden publisering av det humane genom i 2001 og etter den komplette koden fra ett enkelt individ ble kjent i 2007 (første humane diploide genom; dvs. komplett sekvensering av begge kromosomsett), har disse forskningsresultatene lært oss mye om sammenhengen mellom bestemte genkombinasjoner og risiko for sykdomsutvikling. Dette har igjen ført til en kraftig utvikling av markedstilpassede tester.
Utfordringer knyttet til genbasert «helseinformasjon»
Særlig interesse rettes mot gentester som er relatert til forebyggende helsetiltak for individ og samfunn. Et slikt eksempel er de seneste funn av sammenhengen mellom en genetisk markør for leddgikt og den enkeltes forbruk av røyk med eller uten alkohol. Har man arvet denne gensekvensen og røyker, så økes sjansene for utvikling av leddgikt 13 ganger i forhold til den øvrige befolkningen. Inntar man imidlertid samtidig en rimelig mengde alkohol, reduseres sjansen til kun tre ganger i forhold til normalbefolkningen. Den fulle forståelse av mekanismer og sammenheng arbeides det videre med. Leddgikt er en autoimmun lidelse og alkoholens dempende innvirkning på immunsystemet regnes som en sannsynlig forklaring. Disse resultatene illustrerer dessuten det store forskningsbehovet som eksisterer, med hensyn til hvordan denne type opplysninger innvirker på individuelle valg og den offentlige helseforebygging.
Kommersielt press
Det er et betydelig kommersielt press knyttet til muligheter for å tilegne seg og bruke genetisk informasjon og teknologi. Utviklingen går raskt i retning av reduserte priser, forenklede prosedyrer og økt individuell tilgang generelt. Dette kan være et gode for noen, men åpner for en rekke dilemmaer og betenkeligheter når det gjelder ulikhet i bruk og evne til å nyttegjøre seg helsetjenester. Lovgivning, etiske retningslinjer og menneskers holdninger generelt følger til en viss grad den teknologiske utviklingen. Hvordan samfunnet og den enkelte vil forholde seg til, og anvende den nye genteknologien er det ingen klare svar på. Sentralt er blant annet hvilken betydning individuelle data får, for eksempel i spørsmål som angår muligheten for billigere forsikring om det dokumenteres fravær av sykdomsassosierte genmarkører, eller valg av partner/ektefelle etter spesifisert gen-profil.
Hvordan de nye teknologiske muligheter virkelig kommer til å gripe inn i det praktiske samfunnsliv de kommende år er vanskelig å forutse. Imidlertid er det meget sannsynlig at de fleste av oss snart får nærkontakt med den nye teknologien; både som privatpersoner og som yrkesutøvere. Hvordan de nye apotekkjedene og den endrede markedsstrukturen vil forholde seg til de nye muligheter blir spennende å se. I USA formidles for eksempel farskapstester til «hjemmebruk» (til US$ 79 per test) via apoteket. Potensialet er sikkert stort, men kjedene bør være varsomme i sin tilnærming, om ikke dette også skal bli en belastning for apotekets faglige profil.
Etiske spørsmål
Verken forskere, politikere eller befolkningen for øvrig bør forledes til å tro at den stadig økende genteknologiske viten og de mer raffinerte individundersøkelser vil gjøre det særlig lettere å manøvrere mot et sunnere liv eller økt harmoni generelt. Imidlertid vil detaljkunnskap om egen og andres spesifikke genetiske kode sikkert gjøre noemed vårt syn på oss selv og verden. Vi konfronteres med påstanden om at «vår skjebne ligger i genene ...», mens vi undres over hva som er mulig/umulig; bra/ikke ønskelig i forhold til de teknologiske nyvinningene. Refleksjon og debatt rundt dette berører etiske spørsmål, så vel som økonomiske prioriteringer. Innenfor dette komplekse feltet vil sikkert også farmasøyter få en vesentlig utfordring.
(Publisert i NFT, nr. 12/2008 side 18–19.)
