Bivirkningsrapporter fra farmasøyter er viktige
Tekst: Cecilie Sogn Nergård, RELIS Øst,
Oslo universitetssykehus HF, Ullevål
TALL OG FAKTA
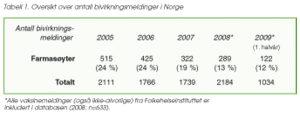
Totalt ble det i Norge i 2008 sendt inn 2184 meldinger om mistenkte bivirkninger, av disse var 289 fra farmasøyter (13 prosent). I Nederland står farmasøyter for ca. 40 prosent av bivirkningsmeldingene. I perioden etter 2005, da frivillig meldeordning for farmasøyter ble innført, har antall meldinger sunket med over 40 prosent, se tabell 1. Selv om en stabilisering av antall rapporter på et lavere nivå var forventet, er det viktig at denne trenden ikke fortsetter.
TYPER MELDINGER FRA FARMASØYTER
Bakgrunnen for å etablere en ordning med bivirkningsrapportering fra farmasøyter var at man ønsket å øke kunnskapen om bivirkninger i preparatgrupper der man erfaringsmessig får få rapporter fra leger og tannleger. Farmasøyter kan få god dialog med kunden om ikke-reseptbelagte legemidler og natur(lege)midler/kosttilskudd, og kan derfor fange opp andre bivirkninger enn de som tradisjonelt rapporteres fra leger.
Ikke-reseptbelagte legemidler og natur(lege)midler/kosttilskudd
I 2008 omhandlet om lag 6 prosent av farmasøytmeldingene ikke-reseptbelagte legemidler eller natur(lege)midler/kosttilskudd. Kun fem meldinger omhandlet plantebaserte produkter. Økt fokus på disse produktgruppene hos farmasøyter kan bidra til viktig og ny kunnskap. Dette gjelder både for bivirkninger og mulige interaksjoner med andre legemidler.
Generisk bytte
De siste årene (2007–2009) har bivirkningsmeldinger ved generisk bytte utgjort mellom 40 og 50 prosent av farmasøytmeldingene. I 2008 omhandlet omtrent 60 prosent av bivirkningsmeldingene på generisk bytte Metoprolol Sandoz. Både manglende effekt, men også bivirkninger assosiert med betablokkere (som kan tyde på for høy dose) ble rapportert etter bytte fra Selo-Zok. Statens legemiddelverk har vurdert disse bivirkningsmeldingene og konkludert med at det ikke er grunn til å gjøre noe med byttelisten i forhold til Metoprolol Sandoz og Selo-Zok.
Legemiddelverket oppfordret i 2003 til å melde fra om bivirkninger og/eller endret effekt, feilbruk og dårlig etterlevelse i forbindelse med likeverdig bytte. Men etter at en stor andel av bivirkningsmeldingene vedrørende likeverdig bytte er gjennomgått, har Legemiddelverket konkludert med at det ikke lenger er nødvendig å ha likeverdig bytte under særlig overvåkning. Alvorlige og uventede bivirkninger i forbindelse med likeverdig bytte bør fortsatt meldes. Ved innsending av slike meldinger er det viktig å få med informasjon om produsent av begge preparatene, og utfallet for pasienten etter eventuelt bytte tilbake til det opprinnelige preparatet.
Reseptbelagte legemidler
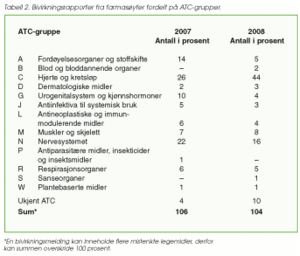
Størstedelen av farmasøytmeldingene gjelder reseptbelagte legemidler. En oversikt over fordelingen på ATC-gruppe er gitt i tabell 2. Økningen i rapporter i ATC-gruppe C (fra 2007 til 2008) skyldes hovedsakelig meldingene på Metoprolol Sandoz.
EKSEMPLER PÅ VIKTIGE BIVIRKNINGSMELDINGER
Interaksjon mellom noskapin og warfarin
Noskapin er et reseptfritt, hostestillende legemiddel som stort sett bare brukes i Skandinavia. Informasjon om stoffets egenskaper er derfor begrenset. På bakgrunn av bivirkningsmeldinger er det nylig oppdaget at noskapin interagerer med warfarin og kan gialvorlig INR-stigning. Denne interaksjonen illustrerer potensialet for alvorlige problemer med preparater som selges uten resept. Apotek bør informere alle som kjøper noskapin om interaksjonsrisiko: Husk at det ikke bare er eldre som bruker warfarin. Apotek bør informere Marevan-brukere om at de må unngå noskapin.
Slimhinneavsvellende nesespray og dråper – bruk hos barn
Legemiddelmyndigheter i USA (FDA) og enkelte EU-land har mottatt meldinger om alvorlige bivirkninger hos små barn ved bruk av legemidler mot forkjølelse (mot hoste, slim eller tett nese). Etter råd fra Bivirkningsnemnda ble det satt fokus på dette også i Norge. Ved uriktig bruk og høy dosering kan absorpsjon gi systemisk effekt og føre til symptomer som hurtig eller ujevn puls, forhøyet blodtrykk og noen ganger bevisshetstap. Legemiddelverket advarer mot bruk av slimhinneavsvellende nesespray og dråper (oksymetazolin eller zylometazolin) hos barn under to år.
Kosttilskudd og leverbivirkninger
Rapporter om leverbivirkninger assosiert med helsekostproduktet Fortodol® førte til analyser av produktet. Dette avslørte et ulovlig tilsatt legemiddel (nimesulid) i terapeutiske doser og produktet ble trukket fra markedet. Nimesulid er et NSAID med kjent leverproblematikk som ikke er godkjent i Norge. Fortodol® ble solgt fra norske helsekostbutikker.
Interaksjon mellom levotyroksin og soyaprodukter
En pasient med overgangsplager hadde behov for stadig større doser Levaxin (levotyroksin) mot sin hypotyreose etter oppstart med et soyaprodukt. Etter seponering av soyaproduktet ble pasientens TSH og T4-verdier normalisert. Data som foreligger tyder på at komponenter i soya kan hemme absorpsjon av levotyroksin. Levotyroksin absorberes nesten fullstendig innen en time etter inntak, men siden tyroideahormonene har enterohepatisk sirkulasjon, kan man ikke utelukke interaksjon selv om man ikke tar soya og levotyroksin samtidig. Ønsker pasienter på levotyroksin å bruke soyaprodukt bør de få beskjed om å informere sin lege for oppfølging av tyroideahormonene, og fortrinnsvis ikke ta produktene samtidig.
VÆR ÅRVÅKEN!
For å oppdage nye bivirkninger er det viktig at helsepersonell er årvåkne og tenker mulighet for bivirkning når uventede reaksjoner oppstår hos pasientene. Det er viktig å huske på at mistanke om sammenheng mellom legemiddel og bivirkning er tilstrekkelig for å sende en bivirkningsmelding.
Kilder
- Statens legemiddelverk. Rapportering av bivirkninger fra farmasøyter 2004 www.legemiddelverket.no/upload/15687/ Brosjyre-14des-trykk.pdf
- RELIS årsrapport 2005-2008. www.relis.no/Kontaktinfo/tabid/56/Default.aspx
- Statens legemiddelverk/RELIS. Årsrapport 2005–2008. www.relis.no/Kontaktinfo/tabid/56/Default.aspx
- Statens legemiddelverk. Den norske bivirkningsdatabasen, søk 10. juli 2009.
- Myhr K. Noskapin og warfarin – en potensielt farlig interaksjon. Tidsskr Nor Legeforen 2009; 129(6): 540.
- Statens legemiddelverk. Kosttilskuddet Fortodol kobles til dødelige leverbivirkninger. www.legemiddelverket.no/templates/InterPage____80684.aspx (publisert25.03.2009)
- Gedde-Dahl A, Harg P et al. Characteristics and quality of adverse drug reaction reports by pharmacists in Norway. Pharmacoepidemiol Drug Saf 2007; 16: 999–1005.
- Statens legemiddelverk. Nesespray og dråper mot nesetetthet anbefales ikke til barn under 2 år. (oppdatert 5. januar 2009)
(Publisert i NFT nr. 11/2009 side 14–15.)
