Hvordan gi råd om bruk av plantebaserte produkter?
* Individuell vurdering
RELIS mottar ukentlig spørsmål fra helsepersonell om bruk av plantebaserte produkter (plantebaserte legemidler og – kosttilskudd) og spesielt om interaksjonspotensial med legemidler. I de fleste tilfellene fraråder vi bruk. Hvorfor gjør vi det?
En systematisk tilnærming for å besvare slike spørsmål kan spare både tid og gjøre det enklere å gi pasientene rasjonelle og begrunnede råd. Før man bruker tid på å undersøke dokumentasjon for det plantebaserte produktet bør man kartlegge om pasienten i utgangspunktet:
- Tilhører en gruppe som bør unngå bruk av plantebaserte produkter
- Bruker legemidler som generelt ikke bør kombineres med plantebaserte produkter.
Figur 1 er et flytskjema som kan følges i samtale med pasienten for å gi råd ved spørsmål om bruk av et plantebasert produkt. Under vil vi utdype rådene.
1. Pasienten
Noen pasienter bør unngå bruk av plantebaserte produkter
For noen pasientgrupper er det spesielt viktig å gjøre en risikovurdering. Dersom pasienten får behandling mot alvorlig sykdom (inkludert kreft), kan en eventuell påvirkning av behandlingen eller sykdomsforløpet få store negative konsekvenser. Vi fraråder derfor alltid pasienter med alvorlig sykdom å bruke plantebaserte produkter. Det samme vil gjelde ved mange kroniske sykdommer. Er man i tvil, bør pasienten diskutere dette med legen sin.
Transplanterte bør ikke bruke plantebaserte produkter, fordi risiko for skade på transplantert organ og avstøtning ikke kan utelukkes.
Redusert organfunksjon (lever/nyre) er en risikofaktor for negative effekter av plantebaserte produkter. Leverbivirkninger er assosiert med plantebaserte produkter (1), og RELIS mottar flere bivirkningsrapporter på dette årlig (2).
Gravide og ammende bør generelt avstå fra bruk av plantebaserte produkter på grunn av manglende dokumentasjon for sikkerhet for fosteret og barnet som ammes.
Små barn er generelt mer utsatt for bivirkninger, for eksempel allergiske reaksjoner, fotosensitisering, dehydrering og elektrolyttforstyrrelser. Eksponering over tid kan være spesielt uheldig for barn på grunn av redusert evne til utskillelse og påfølgende akkumulering. Noen plantebaserte legemidler har godkjent bruksområde for barn (3–7). Dette skal i så fall være spesifisert i pakningsvedlegget (8).
For eldre er det viktig å gjøre en individuell risikovurdering. Generelt er eldre mer utsatt for bivirkninger. Dette skyldes blant annet begrenset fysiologisk reservekapasitet, i form av for eksempel redusert nyrefunksjon, at de oftere har flere lidelser samtidig (komorbiditet) og bruker mange legemidler (9).
Plantebaserte produkter bør ikke brukes 1–2 uker før en operasjon på grunn av mulig økt blødningsrisiko (8).
Rådene om å unngå bruk for disse pasientene kan kanskje oppfattes som konservative og strenge, men bygger på en nytte- og risikovurdering for plantebaserte produkter. Vi mener at nytteverdien svært ofte er for dårlig dokumentert, og at det derfor er problematisk å akseptere risiko, selv om den kan være lav. Risiko er også vanskelig å forutsi, og enkelte pasienter ser ut til å være mer følsomme for bivirkninger enn andre.
Vi mener at plantebaserte produkter kun bør brukes i en begrenset periode, for lettere plager egnet til egenbehandling hos ellers friske personer.
2. Pasientens legemidler
Noen legemidler bør ikke kombineres med plantebaserte produkter
Pasienter med kroniske og alvorlige sykdommer bruker ofte viktige legemidler med uttalte effekter. Redusert effekt av disse kan i verste fall gi terapisvikt, mens økt effekt kan gi bivirkninger. Dersom pasientene blir gjort oppmerksom på mulige konsekvenser, vil det kanskje være enklere for dem å vurdere om bruk av plantebasert produkt er verdt risikoen.
Legemidler med smalt terapeutisk vindu bør ikke kombineres med plantebaserte produkter. Eksempler på slike legemidler er litium, fenytoin, teofyllin, warfarin, digoksin, flere immunosuppressiva inkludert ciklosporin og takrolimus, cytostatika, flere antimykotika, aminoglykosider, med flere (10, 11).
Sammenliknet med warfarin er de nye direkte virkende orale antikoagulasjonsmidlene (DOAK) enklere å dosere og krever ikke regelmessig monitorering med blodprøver (12, 13). DOAK kan derfor oppfattes som tryggere enn warfarin med hensyn til interaksjoner med plantebaserte produkter. Interaksjonspotensialet til DOAK er fremdeles ikke fullstendig klarlagt, og som for warfarin kan interaksjoner medføre potensielt alvorlige komplikasjoner (14, 15). Disse midlene gis også i stor grad til eldre pasienter med komorbiditet. Etter vår vurdering tilhører derfor DOAK en gruppe legemidler som ikke bør kombineres med plantebaserte produkter basert på føre var-prinsippet.
Det er en helt klar relasjon mellom antall samtidig brukte legemidler og risiko for interaksjoner. Pasienter med polyfarmasi er også mer sårbare for uhensiktsmessige effekter av legemidler (16). Det er svært vanskelig å forutsi en mulig effekt av et plantebasert produkt i kombinasjon med et allerede komplekst legemiddelregime, og det bør etter vår vurdering derfor unngås.
3. Plantebaserte produkter
Ulike typer produkter: Plantebaserte legemidler og – kosttilskudd
Et plantebasert legemiddel defineres som ett eller flere virkestoff som er sammensatt av plantemateriale, hvor de virksomme bestanddelene utelukkende består av en eller flere plantedroger eller plantebaserte tilberedninger. De plantebaserte legemidlene har samme krav til kvalitet når det gjelder produksjon, men betydelig reduserte krav til dokumentasjon av effekt og sikkerhet, sammenliknet med legemidler (17). Plantebaserte legemidler godkjennes av Statens legemiddelverk. En oversikt over godkjente plantebaserte legemidler finnes på Legemiddelverkets nettside (18).
Plantebaserte kosttilskudd er juridisk sett matvarer. Mattilsynet har ingen godkjenningsordning for kosttilskudd, men har ansvaret for tilsyn med at regelverk blir fulgt. De som produserer, importerer og selger kosttilskudd har ansvar for at produktene er trygge ved den anbefalte doseringen og at de ikke inneholder helsefarlige stoffer (19). Det er ingen krav til standardisering eller systematisk analyse av det plantebaserte innholdet i et kosttilskudd, og derfor kan innholdsstoffene variere fra produkt til produkt og fra batch til batch. Den store variasjonen i innholdsstoffer og kvalitet er en utfordring når man skal studere effekt og sikkerhet av plantebaserte produkter. Dokumentasjon for ett produkt er ikke nødvendigvis gyldig for andre produkter basert på samme plantemateriale.
På bakgrunn av usikkerheten knyttet til mange plantebaserte kosttilskudd, mener vi at plantebaserte legemidler bør foretrekkes.
Markedsføring og risikoprodukter
Kosttilskudd markedsføres intensivt og omsettes for milliarder hvert år i Norge (20). Det finnes seriøse aktører på markedet som kan ha god kontroll på sine produkter, men det finnes også et stort antall useriøse aktører. Dersom reklame for plantebaserte kosttilskudd lover kraftig og rask effekt, bør man være skeptisk. Plantebaserte stoffer som kan gi slik effekt er i hovedregel klassifisert som legemiddel. Det finnes flere eksempler på at kosttilskudd har vært tilsatt legemidler eller andre stoffer udeklarert (21, 22). Dette gjelder spesielt produkter som selges via internett, og disse betegnes som høyrisikokosttilskudd. Flere ganger har det vist seg at innholdsfortegnelse og produsentomtale ikke stemmer med innholdet i pakningene (23). Erfaringsmessig er risikoen for forurensning med / tilsetning av forbudte stoffer størst for kosttilskudd som påstås å gi økt fysisk eller kognitiv prestasjon, være potensfremmende, smertestillende eller slankende (23, 24).
Interaksjonspotensialet
Både mengden av, og variasjoner i, innholdsstoffene gjør det vanskelig å studere interaksjonspotensialet til plantebaserte produkter. Interaksjoner mellom plantebaserte produkter og legemidler er i liten grad systematisk undersøkt. Det finnes noen få unntak, men kunnskapen kommer sjelden fra kliniske studier. Oftest predikeres potensielle interaksjoner basert på én eller flere rapporterte kasuistikker, dyreforsøk, celleforsøk eller også fra mer hypotetiske betraktninger basert på kjente innholdsstoffer i en plante (25, 26).
Dersom man etter et grundig litteratursøk ikke finner at en interaksjon mellom et plantebasert produkt og et legemiddel er beskrevet, kan det skyldes at det bare ikke er undersøkt eller kjent. Etter vår vurdering bør det derfor uansett alltid frarådes å kombinere et plantebasert produkt med et legemiddel med smalt terapeutisk vindu.
Bivirkninger av plantebaserte produkter
Plantebaserte produkter som selges i Norge, vil som hovedregel ha svake (om noen) effekter, og oftest milde bivirkninger. De fleste matvarer kan gi lette plager med magen eller allergiske reaksjoner, og dette gjelder også for denne typen produkter (8). I Norge er allergiske reaksjoner blant de hyppigst rapporterte bivirkningene for plantebaserte produkter (2), og personer med kjent allergi kan ha økt risiko (8, 26). I sjeldne tilfeller er det rapportert om alvorlige bivirkninger, blant annet alvorlig levertoksisitet og død (1, 27, 28).
Ved mistanke om at et plantebasert produkt har forårsaket bivirkninger eller interaksjoner bør dette meldes til Statens legemiddelverk via RELIS (www.relis.no), på samme måte som for legemidler.
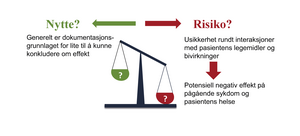
Nytte- og risikovurdering av plantebaserte produkter (figur 2)
For enhver behandling bør en nytte- og risikovurdering ligge til grunn. Når det gjelder plantebaserte produkter, er dokumentasjonen for effekt (nytte) begrenset og ofte fraværende. I mange tilfeller ønsker pasienten å bruke et plantebasert produkt etter råd fra venner og familie (30), eller etter å ha blitt utsatt for massiv markedsføring. Alle helsepåstander som brukes i markedsføringen av kosttilskudd skal være korrekte, de skal kunne dokumenteres og skal ikke villede (31). Dette er dessverre ofte ikke tilfelle (32).
Mange har en oppfatning om at bruk av produkter fra naturen («naturlig») er helt trygt, men det er fortsatt mye vi ikke vet, spesielt om interaksjoner med legemidler. Dersom noe har effekt, vil det også kunne ha bivirkninger. Dersom noe ikke har effekt, er det heller ingen garanti for at produktet ikke kan være skadelig.
Det er krav til faglig forsvarlighet ut fra det en kan forvente på bakgrunn av helsepersonells kvalifikasjoner. Det både er og skal være høye forventninger til faglig kvalifikasjon for farmasøyter (33). Det er problematisk å anbefale produkter med uavklart nytteverdi dersom det samtidig er usikkerhet rundt risiko. Dette er grunnen til at vi i mange tilfeller fraråder bruk av plantebaserte produkter til pasienter.
Farmasøytens rådgivning
Farmasøyter skal bidra til riktig legemiddelbruk og har faglige forutset-ninger for å kunne gi gode råd om bruk av plantebaserte produkter. Spørsmål om plantebaserte produkter kan brukes for å få i gang en samtale der pasienten føler seg sett og tatt på alvor, og for å avdekke viktige problemstillinger.
Hva er bakgrunnen for ønsket om å bruke plantebaserte produkter, ofte i tillegg til legemidler? Er det fordi pasienten ikke har optimal effekt av legemidlene sine eller opplever bivirkninger? Tar pasienten legemidlene sine som forskrevet (etterlevelse/compliance)? Det er i slike tilfeller viktig å sikre at pasienten ikke bytter ut et forskrevet legemiddel med et plantebasert produkt, og gi pasienten rådgivning med sikte på å optimalisere behandlingen. Det kan være å gi råd for å bedre etterlevelsen, om å informere legen om at man ikke tar legemidlet som forskrevet, eller om muligheten for å bytte legemiddel ved intolerable bivirkninger.
Plantebaserte produkter bør kun brukes i en begrenset periode, for lettere plager egnet til egenbehandling hos ellers friske personer. Plantebaserte legemidler bør foretrekkes fremfor plantebaserte kosttilskudd.
Dersom pasientens plager ikke er egnet for egenbehandling, bør pasienten henvises til legen sin.
Referanser
- National Institute of Health (NIH). LiverTox. Herbals and dietary supplements https://livertox.nih.gov/ (Sett: 17. september 2019).
- Nergård CS. Bivirkninger av plantebaserte produkter. Norsk Farmaceutisk Tidsskrift 2013; 7/8: 36–40.
- Nasjonalt kompetansenettverk for legemidler til barn. Bivirkninger. www.legemidlertilbarn.no (Publisert: 12. november 2018).
- Alomar MJ. Factors affecting the development of adverse drug reactions (Review article). Saudi Pharm J 2014; 22: 83–94. doi.org/10.1016/j.jsps.2013.02.003
- Gardiner P. Dietary supplements use in children: Concerns of efficacy and safety. Am Fam Physician 2005; 71: 1068–71.
- Woolf AD. Herbal remedies and children: Do they work? Are they harmful? Pediatrics 2003; 112(S1): 240–6.
- Matportalen. Bør enkelte være spesielt forsiktig med kosttilskudd? www.matportalen.no (Sist endret: 17. november 2017).
- Statens legemiddelverk. Biverknader og råd om bruk av plantebaserte legemiddel. https://legemiddelverket.no/ (Publisert: 23. juni 2016).
- Nyborg G, Straand J et al. Inappropriate prescribing for the elderly – a modern epidemic? Eur J Clin Pharmacol 2012; 68: 1085–94.
- Clinical Pharmacology 2019 database. List of Narrow Therapeutic Index Drugs. Elsevier, Inc. www.clinicalkey.com/pharmacology/login (Sett: 24. september 2019).
- Norsk legemiddelhåndbok for helsepersonell. Søk: smalt terapeutisk vindu. http://legemiddelhandboka.no/ (Søk: 24. september 2019).
- Norsk legemiddelhåndbok for helsepersonell. G 4.1.4. Tabell 4: Mulige legemiddelinteraksjoner ved bruk av DOAK. http://legemiddelhandboka.no/ (Søk: 24. september 2019).
- Eek AK, Strøm BO et al. Bivirkninger ved bruk av antikoagulasjonsmidler i 2013–15. Tidsskr Nor Legeforen 2018; doi: 10.4045/tidsskr.17.0706
- Pettersen PM. DOAK-interaksjoner øker risiko for blødning. Tidsskr Nor Legeforen 2017; doi: 10.4045/tidsskr.17.0907
- Di Minno A, Frigerio B et al. Old and new oral anticoagulants: Food, herbal medicines and drug interactions. Blood Rev. 2017; 31: 193–203.
- Rognstad S. Mange legemidler til eldre – det er fali’, det. Tidsskr Nor Legeforen 2014; 134: 1016.
- Fleiner HF. Roland PDH. Plantebaserte produkter – hva vet vi? Utposten 2017; 46: 52–4.
- Statens legemiddelverk. Tradisjonelle og veletablerte plantebaserte legemidler med markedsføringstillatelse. https://legemiddelverket.no/ (Sist oppdatert: 5. september 2019).
- Mattilsynet. Kosttilskudd. www.mattilsynet.no (Sist endret: 12. august 2018).
- Nasjonalt forskningssenter innen komplementær og alternativ medisin. Tallene fra NAFKAM-2018 er klare: Nordmenn bruker fortsatt mye alternativ behandling. https://nafkam.no (Publisert: 27. jui 2019).
- Helle C, Sommer AK et al. Dopingmidler i kosttilskudd. Tidsskr Nor Legeforen 2019; doi: 10.4045/tidsskr.18.0502
- Matportalen.no. Kosttilskudd og helsekost kjøpt via Internett. www.matportalen.no/ (Sist endret: 24. januar 2018).
- Matportalen.no. Vær kritisk til urtebasert kosttilskudd. www.matportalen.no/ (Sist endret: 14. november 2017).
- Mattilsynet. Tilsynsrapport: Kosttilskudd kan inneholde ulovlige og helsefarlige stoffer. www.mattilsynet.no (Sist endret: 30. november 2012).
- Werba JP, Misaka S et al. Update of green tea interactions with cardiovascular drugs and putative mechanisms. J Food Drug Anal 2018; 26: S72–S77.
- Izzo AA, Hoon-Kim S et al. Critical Approach to Evaluating Clinical Efficacy, Adverse Events and Drug Interactions of Herbal Remedies. Phytother Res 2016; 30: 691–700.
- European Food Safety Authority. EFSA assesses safety of green tea catechins. www.efsa.europa.eu/ (Publisert: 18. april 2018).
- Navarro V, Khan I et al. Liver Injury from Herbal and Dietary Supplements. Hepatology 2017; 65: 363–73.
- Vorren S. Alvorlige leverbivirkninger kobles til kosttilskuddet Fortodol. https://relis.no/ (Publisert: 26. februar 2009).
- Krogstad T. Bruk av kosttilskudd, plantebaserte legemidler og naturlegemidler i Norge. Norsk Farmaceutisk Tidsskrift 2011; 12: 26–9.
- Matportalen.no. Kosttilskudd. www.matportalen.no/ (Sist endret: 5. oktober 2017).
- Brean A. Rot i medisinskapet. Tidsskr Nor Legeforen 2019. doi: 10.4045/tidsskr.19.0312
- Helsedirektoratet. Helsepersonelloven med kommentarer: Krav til helsepersonells yrkesutøvelse. www.helsedirektoratet.no (Sist oppdatert: 28. juni 2018).
(Publisert i NFT nr. 8/2019 side 31–33)
