Farmakokinetiske legemiddelinteraksjoner ved behandling med amiodaron (1)
Sammendrag
Hensikt
Hensikten med prosjektet var å identifisere farmakokinetiske interaksjoner med amiodaron, og undersøke håndtering av disse via et tverrfaglig samarbeid mellom farmasøyt og kardiolog på en hjertemedisinsk avdeling.
Materiale og metode
Farmasøyt foretok legemiddelgjennomganger for 25 pasienter som alle ble behandlet med amiodaron ved innleggelse eller under sykehusoppholdet. Tre ulike elektroniske databaser ble benyttet til identifisering av amiodaroninteraksjoner. Et standardisert skjema ble benyttet til registrering av opplysninger fra databasene, innspill fra farmasøyt og legens beslutning i det enkelte tilfelle. Ved intravenøs (i.v.) behandling med amiodaron igangsatt på sykehuset, ble pasienter som brukte warfarin fulgt opp med INR-målinger under hele sykehusoppholdet.
Resultat
For de 25 pasientene ble det i alt gitt 54 innspill fra farmasøyt som omhandlet farmakokinetiske interaksjoner med amiodaron, hvorav 41 (76 %) ble tatt til følge / tatt til etterretning av legen. Innspillene førte til dosereduksjon i 20 tilfeller (49 %), skifte av preparat i 8 tilfeller (20 %) og monitorering av blodverdier i 9 tilfeller (22 %). Pasientkasuistikker viste at interaksjoner også kan oppstå etter i.v. korttidsbehandling med amiodaron. INR-verdiene steg raskt etter bare en dose 150 mg amiodaron hos samtlige pasienter (tre stykker) som ble behandlet med denne kombinasjonen.
Konklusjon
Studien viser at bruk av amiodaron ofte medfører farmakokinetiske interaksjoner med andre legemidler, også ved i.v. korttidsbehandling. Farmasøyt kan i stor grad bidra til å fange opp og forebygge uheldige konsekvenser av interaksjoner hos pasienter som behandles med amiodaron.
Hovedbudskap
Samtlige pasienter som ble behandlet med amiodaron brukte legemidler med potensial for interaksjoner med preparatet.
Interaksjoner kan også oppstå etter intravenøs dosering av amiodaron og medføre usikker og variert legemiddeleffekt over en periode.
Farmasøyter kan bidra til å fange opp og forebygge uheldige konsekvenser av interaksjoner med amiodaron.
Summary, research article
Pharmacokinetic drug-drug interactions involving amiodarone
Aim
The purpose of this study was to identify and submit pharmacist-initiated proposals for handling of drug- drug interactions (DDIs) involving amiodarone in patients admitted to a hospital ward.
Material and Methods
Prior to ward rounds, a pharmacist carried out medication reviews to identify amiodarone DDIs by the aid of electronic databases. Physicians were alerted about DDIs classified in the databases to be of potential clinical relevance («avoid» or «precautions»). Moreover, advices to manage the DDIs were provided by the pharmacist. In addition, in warfarin-treated patients subjected to short-term intravenous amiodarone therapy, INR and warfarin dosing was closely monitored.
Results
Overall, 25 patients were included in the study. The pharmacist identified 54 DDIs of potential relevance involving amiodarone (mean 2.2 DDIs per patient). These DDIs were notified to the physicians, who initiated drug changes or monitoring actions 41 of the cases (76%). In a warfarin-treated patient starting intravenous, short-term amiodarone therapy, INR was raised about two-fold immediately following coadministration of the drugs.
Conclusion
Amiodarone is frequently involved in DDIs in hospitalized patients. Pharmacist could aid the management of these DDIs to avoid or reduce the risk of adverse drug reactions. Health care professionals should be aware that intravenous, short-term amiodarone therapy administered during hospitalization may result in clinically relevant DDIs – at least in patients treated with warfarin.
Last ned hele artikkelen som pdf
Bakgrunn og hensikt
Amiodaron er et potent antiarytmikum som benyttes ved livstruende eller sterkt invalidiserende arytmier, spesielt atrieflimmer. Med sin komplekse farmakokinetikk er preparatet et legemiddel som tydelig synliggjør at farmakokinetiske interaksjoner oppstår og at dette må vurderes i videre behandling av pasienter for å unngå bivirkninger (1). Preparatet metaboliseres via cytokrom P450 3A4 (CYP3A4) til metabolitten desetylamiodaron. Denne hovedmetabolitten har også antiarytmiske egenskaper, og ved langtidsbehandling er plasmakonsentrasjonen av metabolitten like høy som plasmakonsentrasjonen av amiodaron (2). Eliminasjonen av preparatet er varierende og langsom med halveringstid på 20–100 dager. Både amiodaron og desetylamiodaron har vist seg å være målbare i plasma minst tre måneder etter avsluttet behandling.
Både amiodaron og desetylamiodaron er beskrevet å hemme CYP1A2, CYP2C9, CYP2D6 og CYP3A4, noe som kan resultere i forhøyede plasmakonsentrasjoner av mange andre legemidler ved kombinasjonsbehandling (3). Amiodaron hemmer også transportproteinet permeabilitets glykoprotein (P-gp) i tarm og blod-hjernebarriere, noe som kan medføre økt plasmakonsentrasjon og økt konsentrasjon i sentralnervesystemet (CNS) av P-gp-substrater (2).
De farmakokinetiske egenskapene til amiodaron vil kunne medføre interaksjoner med flere aktuelle legemidler innen hjerte/kar-behandlingen. Preparatet påvirker blant annet warfarin som synliggjøres i form av økt INR-verdi og blødningsrisiko, ved hovedsakelig å hemme metabolismen av S-warfarin via CYP2C9, men også metabolismen av R-warfarin via hemming av CYP3A4 og CYP1A2 (4). Videre er -simvastatin og atorvastatin hyppig brukte statiner som begge metaboliseres via CYP3A4. Kombinasjon med legemidler som hemmer dette enzymet er beskrevet å forårsake myopati og mer sjelden rhabdomylose (5). Digitoxin er på sin side et P-gp-substrat og inntak av kombinasjonen amiodaron og digitoxin / digoxin er rapportert å kunne medføre digitalisforgiftning med blant annet påfølgende arytmier og variabel serumkonsentrasjon (6, 7). Den mest benyttede betablokkeren, metoprolol, blir metabolisert via CYP2D6, og er nok et eksempel der kombinasjonsbehandling med amiodaron vil øke plasmakonsentrasjon og effekt (8).
Hensikten med dette prosjektet, som dannet utgangspunkt for en masteroppgave i klinisk farmasi, var å identifisere amiodaroninteraksjoner og fasilitere håndtering av disse på en hjertemedisinsk avdeling.
Materiale og metode
Studien ble vurdert av Regional komité for medisinsk og helsefaglig forskningsetikk (REK) til ikke å være fremleggingspliktig. Behandling av pasientdata ble deretter godkjent av Norsk samfunnsvitenskapelig datatjeneste (NSD), som har personvernombudfunksjon for Helse Vest RHF. Prosjektet ble utført ved kardiologisk seksjon ved Haugesund sjukehus, Helse Fonna HF.
Ved oppstart ble det holdt fellesundervisning for legene på klinikken hvor tema var farmakokinetiske legemiddelinteraksjoner med spesiell fokus på utfordringer ved amiodaronbehandling. Inneliggende pasienter som enten startet opp eller var under behandling med amiodaron, ble inkludert i perioden fra august til november 2011.
For alle de inkluderte pasientene ble det foretatt en strukturert legemiddelgjennomgang basert på legemiddelkurve, pasientjournal og søk i tre interaksjonsdatabaser, (www.interaksjoner.no (DRUID), Lexi-Interact og www.drugs.com). Interaksjoner klassifisert som «Bør unngås» eller «Ta forholdsregler» i DRUID, grad C, D og X i Lexi-Interact, og «Major» eller «Moderate» i drugs.com, ble registrert på eget skjema. I forbindelse med previsitter opplyste farmasøyten om aktuelle interaksjoner av potensiell klinisk betydning og ga innspill til lege om mulig håndtering for å unngå/forebygge legemiddelrelaterte problemer. Alle identifiserte legemiddelinteraksjoner som involverte amiodaron, samt innspill fra farmasøyt til lege og legens beslutning i det enkelte tilfelle, ble registrert på et utarbeidet pasientskjema. På forhånd var det – basert på søk i PubMed og andre databaser – innhentet informasjon om aktuelle håndteringstiltak («løsninger») for utvalgte legemidler som blir påvirket interaksjonsmessig av amiodaron, det vil si warfarin, digitoxin, simvastatin, atorvastatin og metoprolol. Det ble i prosjektet også gitt innspill om identifiserte interaksjoner som omfattet andre legemidler enn amiodaron, men opplysninger rundt og håndtering av disse ble ikke registrert.
I tillegg til registrering av påviste interaksjoner og iverksatte håndteringstiltak, ble det i prosjektet gjort forsøk på å evaluere amiodarons interaksjonspotensial ved intravenøs korttidsbehandling. Dette ble undersøkt for warfarinbehandlede pasienter, der INR-verdiene ble fulgt under sykehusoppholdet etter intravenøs administrering av amiodaron.
Resultater
Totalt ble 25 pasienter inkludert i prosjektet (tabell 1). Av disse ble 13 pasienter behandlet med amiodaron før sykehusoppholdet, mens hos 12 pasienter ble amidaronbehandling igangsatt etter innleggelse. For samtlige av de inkluderte pasientene ble det ved databasesøk identifisert en eller flere potensielle interaksjoner som involverte amiodaron. Gjennom søk i DRUID ble det detektert 49 (gjennomsnittlig 1,96 per pasient) amiodaroninteraksjoner, mens tilsvarende tall var 80 (3,2 per pasient) for drugs.com og 91 (3,6 per pasient) for Lexi-interact. Totalt ble det identifisert 36 legemidler som kunne skape interaksjonsproblematikk med amiodaron. De hyppigste var metoprolol (13 pasienter), warfarin (9 pasienter), simvastatin (9 pasienter) og digitoxin (7 pasienter).

Det ble gitt 54 innspill (gjennomsnitt 2,2 innspill per pasient) til behandlende lege vedrørende interaksjonsproblematikk med amiodaron. Av disse ble 41 tilfeller (76 %) tatt til følge i form av forskrivningsendringer eller monitoreringstiltak (figur 1). To tredjedeler av innspillene som ble gitt omhandlet de fire mest brukte legemidlene. Dosereduksjon utgjorde halvparten av alle innspill som ble tatt til følge, enten i forbindelse med oppstart eller justering av tidligere igangsatt legemiddelbehandling.
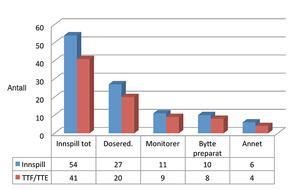
Kombinasjonen warfarin-amiodaron nødvendiggjorde reduksjon av warfarindose for 5 av 9 pasienter, mens dose digitoxin ble redusert for 3 av 7 pasienter. Det var 15 pasientene som brukte simvastatin eller atorvastatin i kombinasjon med amiodarone. Blant disse fikk 7 pasienter statindosen redusert, mens 3 pasienter skiftet statinpreparat. Videre ble dose metoprolol redusert for 6 av 13 pasienter som fikk dette legemidlet i kombinasjon med amiodarion.
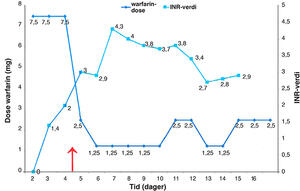
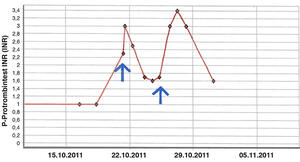
I alt tre pasienter ble behandlet med kombinasjonen warfarin og amiodaron intravenøst. Endring i INR-verdi og warfarindosering etter oppstart av kombinasjonsbehandling for to av disse pasientene er illustrert i figur 2 a og b. Etter oppstart av korttidsbehandling med amiodaron under sykehusoppholdet steg INR-verdi til om lag det dobbelte kort tid etter oppstart av kombinasjonsbehandling. For å kompensere for dette ble dose warfarin redusert tilsvarende.
Diskusjon
Denne studien ble begrenset til å gjelde interaksjoner med amiodaron, som har et stort interaksjonspotensial med andre legemidler. Dette ble illustrert ved at det ble funnet gjennomsnittlig to klinisk relevante interaksjoner per pasient. Studien viste høy legeaksept på farmasøytens innspill, enten i form av justering/endring av behandling eller igangsetting av monitoreringstiltak. Denne studien ga ikke mulighet for å evaluere den kliniske nytteverdien av intervensjonene, men tidligere studier har vist at innspill fra farmasøyt kan bedre pasientsikkerheten og i tillegg gi økonomisk gevinst (9).
Tall fra Norge viser at opptil 9 % av inneliggende pasienter har klinisk relevante interaksjoner i løpet av behandlingstiden (10). Håndtering og forebygging av interaksjoner i forbindelse med sykehusopphold kan derfor bidra til færre bivirkninger og bedre behandlingsrespons både under og etter oppholdet (11). Amiodaron er et antiarytmikum der behandling initieres på sykehus, enten permanent eller i en kort periode. I denne studien gjennomgikk rundt halvparten av de inkluderte pasientene korttidsbehandling med amiodaron under sykehusoppholdet. Tre av disse pasientene ble samtidig behandlet med warfarin, og monitorering av INR viste at amiodaron kan medføre betydelige interaksjoner også ved kortvarig administrering.
For å unngå høye INR-verdier ble warfarindosen redusert hos 5 av 9 pasienter der preparatet ble kombinert med amiodaron. Med bakgrunn i tidligere studier som har vist en 3–4 gangers økt risiko for blødninger når warfarin kombineres med en CYP2C9-hemmer, og at halvparten av alle blødningsreaksjonene ved warfarin skyldes interaksjoner med andre legemidler, er det fornuftig å redusere dose warfarin i forkant av en forventet interaksjonen (4, 12). Alternativt kan man behandle med en annen koagulasjonshemmer i stedet, for eksempel dabigatran. Ettersom dabigatran er et substrat for transportproteinet P-glykoprotein (Pgp), som også amiodaron hemmer aktiviteten av, er det imidlertid en teoretisk risiko for økt effekt av dabigatran i kombinasjon med amiodaron.
Digitoxin og digoxin er substrater av Pgp. Samtidig inntak av amiodaron er rapportert å medføre digitalisforgiftning med blant annet påfølgende arytmier (13). På grunn av kort liggetid på sykehuset og liten grad av serum monitorering av digitoxin, var det ikke mulig å studere eventuell effekt av interaksjonen i prosjektperioden. Med bakgrunn i litteratur ble det likevel anbefalt å halvere dosen digitalisglykosider ved oppstart av amiodaron. Man må være spesielt oppmerksom på at serumkonsentrasjon ikke nødvendigvis korrelerer med konsentrasjon i annet vev, og det er nødvendig med økt forskning in vivo for i større grad å kunne forutsi en eventuell betydning av hemming av Pgp i hjernen for toksisitet av digitoxin/digoxin.
Simvastatin og atorvastatin er både substrater for CYP3A4 og Pgp, og kombinert bruk av amiodaron kan medføre betydelige økninger i serumkonsentrasjon og risiko for bivirkninger av begge statiner. Interaksjon mellom amiodaron og simvastatin/atorvastatin var generelt lite kjent blant legene. Andre studier har tilsvarende vist at leger i liten grad følger opp statinbehandingen når pasienter starter behandling med nye legemidler (15). Nærmere halvparten av pasientene som får foreskrevet amiodaron bruker et statin, og man bør derfor være oppmerksom på denne interaksjonsrisikoen og enten redusere statindose eller benytte et ikke-interagerende statin (14). Generelt anbefales det at dosen av simvastatin ikke bør overstige 20 mg daglig i kombinasjon med hemmere av CYP3A4, mens det tilsvarende ikke foreligger noen klar doseanbefaling for atorvastatin (5).
Kombinasjonen mellom amiodaron og metoprolol er også ganske vanlig. De fleste leger vet at disse legemidlene forsterker hverandres effekt farmakodynamisk, men få er klar over at amiodaron øker serumkonsentrasjonen av metoprolol. Flere studier har vist at dosen av metoprolol ved oppstart av amiodaron bør halveres på grunn av den farmakokinetiske interaksjonen (8).
Tidlig i prosjektperioden ble det tydelig at mulig interaksjonsrisiko ved intravenøs behandling med amiodaron var noe legene i liten grad anså som relevant, til tross for preparatets lange halveringstid. De tilfeller der INR-verdi hos warfarinpasienter ble fulgt etter enkeltdosering av amiodaron intravenøst, viste at påvirkningen av amiodaron inntrådte raskt og vedvarte relativt lenge. En langvarig interaksjonseffekt er i tråd med en studie utført av Holt et al. som viste at halveringstiden av amiodaron er på 20–47 dager etter administrering av en intravenøs støtdose av preparatet (150 mg) hos friske personer (2). Effekten av interaksjonen kan følgelig være aktuell opptil tre måneder etter korttids dosering/seponering av amiodaron. Dette understøttes av Lu et al., som i en studie viste at man etter oppstart av amiodaron i kombinasjon med warfarin først ser stabil INR-verdi etter 12 uker (1).
Amiodarons lange halveringstid innebærer at oppfølging av interaksjoner med preparatet er høyst nødvendig også etter utskriving fra sykehus. Det er derfor viktig at påviste interaksjoner beskrives nøye i epikrisene, slik at fastlegene har et godt utgangspunkt for videre oppfølging og eventuelt dosejustering av legemidler som påvirkes av amiodaron. Preparatet bør også føres i legemiddelkurve når pasienten er behandlet på annet sykehus med amiodaron rett før aktuell innleggelse for å være oppmerksom på interaksjonsproblematikk videre i behandlingen.
I prosjektet ble det benyttet tre ulike interaksjonsdatabaser. Søk i databasene ga ulike resultater når det gjaldt amiodaroninteraksjoner. Interaksjonene oppgitt i DRUID var totalt sett færre sammenliknet med de to andre databasene, men funn i DRUID ble av farmasøyten ansett som mer relevante i forhold til pasientbehandlingen. Erfaringene fra prosjektet var imidlertid at søk i flere databaser samlet sett ga et verdifullt grunnlag for vurdering og håndtering av identifiserte interaksjoner. Selv om tilgang på gode databaser er nødvendig, er også farmakologisk og terapeutisk kunnskap, situasjonsforståelse, og god samhandling/kommunikasjon mellom farmasøyt og lege viktige faktorer for å oppnå en effektiv og god interaksjonshåndtering.
Konklusjon
Amiodaron er et legemiddel med stort potensial til å interagere med andre legemidler gjennom multiple mekanismer. Denne studien viste at kombinasjonsbehandling med interagerende legemidler er hyppig forekommende blant hjertepasienter innlagt på sykehus. Samtlige pasienter som ble behandlet med amiodaron brukte legemidler med potensial for interaksjoner med preparatet. Endringer eller monitoreringstiltak ble iverksatt i de aller fleste tilfellene etter at farmasøyt hadde varslet lege. Dette viser at tverrfaglig samarbeid mellom lege og farmasøyt kan være effektivt for å forebygge alvorlige reaksjoner som følge av amiodaroninteraksjoner. Det ble i prosjektet også vist at kortvarig, intravenøs amiodaronbehandling kan medføre betydelige INR-økninger hos pasienter behandlet med amiodaron. Helsepersonell bør derfor være oppmerksom på interaksjonsfaren med amiodaron ved kortvarig behandling på sykehus.
Oppgitte interessekonflikter: Ingen
Referanser
- Lu Y, Won KA, Nelson BJ et al. Characteristics of the amiodarone-warfarin interaction during long-term follow-up. Am J Health Syst Pharm 2008; 65: 947–52.
- Holt DW, Tucker GT, Jackson PR et al. Amiodarone pharmacokinetics. Br J Clin Prac Suppl 1986; 44: 109–14.
- Ohyama K, Nakajima M, Suzuki M et al. Inhibitory effects of amiodarone and its N-deethylated metabolite on human cytochrome P450 activities: prediction of in vivo drug interactions. Br Journal Clin Pharmacol 2000; 49: 244–53.
- Hauta-Aho M, Tirkkonen T, Vahlberg T et al. The effect of drug interactions on bleeding risk associated with warfarin therapy in hospitalized patients. Ann Med 2009; 41: 619–28.
- Marot A, Morelle J, Chouinard VA et al. Concomitant use of simvastatin and amiodarone resulting in severe rhabdomyolysis: a case report and review of the literature. Acta clinica Belg 2011; 66: 134–6.
- DeVore KJ, Hobbs RA. Plasma digoxin concentration fluctuations associated with timing of plasma sampling and amiodarone administration. Pharmacotherapy 2007; 27: 472–5.
- Laer S, Scholz H, Buschmann I et al. Digitoxin intoxication during concomitant use of amiodarone. Eur J Clin Pharmacol 1998; 54: 95–6.
- Fukumoto K, Kobayashi T, Tachibana K et al. Effect of amiodarone on the serum concentration/dose ratio of metoprolol in patients with cardiac arrhythmia. Drug metab pharmacokinet 2006; 21: 501–5.
- Bergkvist Christensen A, Holmbjer L, Midlov P et al. The process of identifying, solving and preventing drug related problems in the LIMM-study. Int J Clin Pharm 2011; 33: 1010–8.
- Blix HS, Viktil KK, Reikvam A et al.
The majority of hospitalised patients have drug-related problems: results from a prospective study in general hospitals.
Eur J Clin Pharm 2004; 60: 651–8. - Moura CS, Acurcio FA, Belo NO. Drug-drug interactions associated with length of stay and cost of hospitalization. J Pharm Pharm Sci 2009; 12: 266–72.
- Gasse C, Hollowell J, Meier CR et al. Drug interactions and risk of acute bleeding leading to hospitalisation or death in patients with chronic atrial fibrillation treated with warfarin. Thrombosis and haemostasis 2005; 94: 537–43.
- Grimm W. Bidirectional ventricular tachycardia due to digitalis intoxication. Z Kardiol 2005; 94: 79–80.
- Borders-Hemphill V. Concurrent use of statins and amiodarone.
Consult Pharm 2009; 24: 372–9. - Devold HM, Molden E, Skurtveit S et al. Co-medication of statins and CYP3A4 inhibitors before and after introduction of new reimbursement policy. Br J Clin Pharmacol 2009; 67: 234 –41.
Manuskriptet ble mottatt 23. mars 2012 og godkjent 3. september 2013.
Fotnote:
- Denne artikkelen er basert på en erfaringsbasert masteroppgave i klinisk farmasi ved Universitetet i Oslo (eksamen avlagt februar 2012). Hovedveileder for oppgaven var professor Hege Christensen.
Norsk Farmaceutisk Tidsskrift 2013; 12: 28–32.
